- Головна
- /
- Статті
- /
- Кардіологія
- /
- Проблеми оптимізації медичного застосування β-адреноблокаторів лікарями загальної практики
Проблеми оптимізації медичного застосування β-адреноблокаторів лікарями загальної практики
Бета-адреноблокатори (БАБ) використовуються у медичній практиці понад 40 років. Перші представники цієї групи поряд із діуретиками стояли у витоків доказової медицини й кардіології зокрема. Протягом 80-90-х років ХХ століття у низці рандомізованих подвійних сліпих плацебо-контрольованих досліджень було доведено ефективність застосування препаратів групи БАБ у хворих на артеріальну гіпертензію (АГ), гострий інфаркт міокарда (ІМ), хронічну серцеву недостатність (ХСН) тощо для зменшення кількості серцево-судинних подій і смертності [1, 2, 6, 8, 33, 37, 38].
Однак рівень використання БАБ у лікуванні серцево-судинних захворювань залишається недостатнім. Так, в італійському дослідженні GISSI-Prevenzione (2002; n=2836) тільки 44% пацієнтів отримували БАБ у перші 3 місяці після перенесеного ІМ. Окрім того, слід зазначити, що значна частина хворих отримують БАБ у нецільовій дозі (див. розділ «Показання для застосування»). Головними причинами цього є:
- широкий перелік можливих побічних реакцій (ПР), загрозливість яких часто перебільшується (див. розділ «Побічні реакції на препарати групи БАБ»);
- надмірне ускладнення класифікацій БАБ за рахунок маловагомих додаткових властивостей на кшталт мембраностабілізуючої активності, наведення незареєстрованих в Україні препаратів або лікарських засобів (ЛЗ), які втратили клінічне значення тощо; наявність великої кількості генериків з різною біо- та терапевтичною еквівалентністю;
- повільне впровадження у практику лікарів першої ланки стандартів лікування, навіть затверджених директивно [7].
Досягнення проміжних критеріїв ефективності лікування (показники артеріального тиску [АТ], частоти серцевих скорочень [ЧСС] тощо) [7] за рахунок ЛЗ із достовірною доказовою базою, якими, зокрема, є БАБ, сприятиме зменшенню кількості ускладнень і загальної смертності серед пацієнтів із серцево-судинними захворюваннями, на відміну від критерію «суб’єктивного полегшення», що досягається шляхом призначення ЛЗ із часто недоведеним ефектом (коронаролітики, метаболічні препарати).
Препарати порівняння
Для порівняння обрано три представники селективних БАБ без внутрішньої симпатоміметичної активності та інших додаткових властивостей – атенолол, метопролол і бісопролол (табл. 1) із таких міркувань:
- наявність β1-адреноселективності, за рахунок якої знижується ризик екстракардіальних ПР при збереженні позитивного впливу на міокард [2, 3];
- відсутність внутрішньої симпатоміметичної активності, яка істотно знижує антиангінальний та кардіопротекторний ефекти БАБ [1, 2, 22, 40, 41];
- тривалий досвід клінічного використання (близько 30 років для атенололу й метопрололу і 20 – для бісопрололу) та значний обсяг якісних клінічних досліджень (див. розділ «Показання для застосування»);
- невисока вартість та широкий ціновий вибір між препаратами різних виробників;
- ці ЛЗ добре відомі вітчизняним клініцистам.
Показання для застосування
Натепер перелік показань для застосування БАБ з позицій доказової медицини має такий вигляд.
Класи рекомендацій:
І – докази і/або висновок експертів свідчать про ефективність та користь втручання;
ІІ – суперечливі дані;
ІІа – співвідношення на користь ефективності;
ІІb – співвідношення свідчить про нижчу ефективність;
ІІІ – докази неефективності або шкідливості втручання.
Рівні доказовості:
А – результати численних рандомізованих клінічних досліджень або метааналізів;
В – результати одного рандомізованого клінічного дослідження або кількох нерандомізованих;
С – висновок експертів і/або дані невеликих досліджень.
Критерієм досягнення цільової дози БАБ є зниження ЧСС принаймні до 55-60 уд/хв у спокої (і навіть нижче в разі гарної переносимості) [1, 22, 23, 40, 41], а критерієм початку β-адреноблокуючої дії – зниження ЧСС на 20-25% від вихідної або розвиток атріовентрикулярної (АV) блокади І ступеня (РQ>0,21 с).
Артеріальна гіпертензія
БАБ є препаратами першого ряду (клас рекомендацій І, рівень доказовості А) для зменшення ускладнень (ішемічної хвороби серця [ІХС], у т.ч. гострого коронарного синдрому [ГКС], ХСН, раптової серцевої смерті [РСС]; мозкового інсульту), зниження рівня кардіальної і загальної смертності у пацієнтів з АГ [1, 11-13]. З урахуванням поширеності АГ в Україні (за даними 2005 р. — понад 10 млн осіб [31]), переносимості БАБ у дієвих дозах більше ніж 80% популяції та найнижчої поряд із діуретиками вартості серед груп ЛЗ першого вибору, цільова група пацієнтів для отримання БАБ становитиме декілька мільйонів осіб [10], оскільки в нашій країні лише від 5 до 15% хворих з АГ отримують адекватну терапію (досягають цільового АТ) [17, 20].
У ранніх дослідженнях (НЕР [1988], MAPHY [1989], HAPPY [1987], STOP-Нypertension [1991]) БАБ достовірно перевершували плацебо і були зіставні з тіазидними діуретиками щодо профілактики серцево-судинних подій (смерть, ІМ, мозковий інсульт) у пацієнтів із підвищеним АТ [33, 37-39]. Пізніші подвійні сліпі плацебо-контрольовані клінічні дослідження (трайли) показали ефективність низки БАБ щодо зниження смертності від усіх причин порівняно з іншими класами препаратів: інгібіторами ангіотензинперетворювального ферменту (ІАПФ) або антагоністами кальцію (STOP-2, 1994) [8, 9], зокрема ІАПФ каптоприлом (САРРР, 1999; UKPDS, 1998) [1, 34] та антагоністами кальцію лацидипіном (ELSA, 2001) [8, 9] і дилтіаземом (NORDIL, 2000), а також верапамілом і діуретиками (CONVINCE, 2003) [8, 13, 14, 36].
Лише у новіших великих трайлах LIFE (2002) та ASCOT-BPLA (2005; n=19257) БАБ поступалися відповідно антагоністу рецепторів ангіотензину ІІ лозартану за кількістю мозкових інсультів та комбінації ІАПФ+антагоніст кальцію за кількістю серцево-судинних подій та рівнем загальної смертності [18, 35].
Також реєструвалася більша кількість випадків уперше виявленого цукрового діабету (ЦД) при застосуванні атенололу, метопрололу й неселективного пропранололу порівняно з ІАПФ та антагоністами кальцію (але не з діуретиками), імовірно за рахунок β2-адреноблокади [2, 4]. Високоселективний бісопролол практично не впливав на показники глікемії у великих дослідженнях СІВІS ІІ і ІІІ протягом приблизно 15 міс спостереження [27, 33]. У дослідженні UKPDS (1998) при лікуванні АГ у хворих на інсуліннезалежний ЦД атенолол не поступався ІАПФ каптоприлу за кількістю серцево-судинних подій, однаковими були також частота епізодів гіпоглікемії та рівень глікозильованого гемоглобіну через 8 років спостереження [34]. Загалом БАБ навіть перевершують ЛЗ таких груп, як антагоністи кальцію та діуретики, щодо ефективності при АГ у хворих на ЦД 2 типу [13].
У метааналізі результатів лікування АГ, проведеному шведськими дослідниками (2004), продемонстровано недостовірний вплив атенололу на кінцеві точки порівняно із плацебо або відсутністю лікування (n=6825) і більшу кількість випадків мозкового інсульту та смерті порівняно з іншими класами ЛЗ – діуретиками, ІАПФ, антагоністами рецепторів ангіотензину ІІ та антагоністами кальцію (n=17 671) [15]. У їхньому метааналізі 2005 р. (13 рандомізованих трайлів, n=105 951) показано дещо вищу смертність у групі БАБ (відносна – на 3%, р=0,14) та достовірно більшу кількість інсультів (на 16%) порівняно з препаратами інших груп [39].
Однак пропозиція виключити БАБ із числа антигіпертензивних ЛЗ першого ряду на основі даних метааналізів зустрічає кілька вагомих застережень:
- немає даних про досягнутий в обох групах рівень зниження АТ: у найбільшому з аналізованих трайлів ASCOT-BPLA (2005; n=19 257) група БАБ+діуретики програвала за цим показником групі ІАПФ+антагоністи кальцію (на 2,7-1,9 мм рт. ст.) [18], хоча за результатами трайлу АLLHAT (2003) менший позитивний вплив ІАПФ пояснено меншим зниженням АТ у цій групі (приблизно на 2 мм рт. ст.) [24];
- у 63% хворих із групи БАБ використано атенолол, інші БАБ були менш ефективними за препарати порівняння щодо попередження мозкового інсульту і більше – щодо зниження частоти ІМ та загальної смертності [16];
- кратність застосування атенололу (разово на добу) та частини інших БАБ (пропранолол, піндолол двічі на добу, ацебутолол разово) не забезпечувала рівномірності антигіпертензивної дії – співвідношення найбільшого ефекту ЛЗ до кінцевого (перед наступною дозою) Т/Р («пік-корито») становило менше 50%. Так, в ASCOT-BPLA індекс Т/Р для комбінації атенолол+діуретики становив 35-40% на противагу 75-90% для ІАПФ+антагоністи кальцію, чим також можна пояснити відносне зниження смертності в останній групі на 12% протягом 4 років [18, 23]. Доведена перевага над плацебо метопрололу (призначали у формі сукцинату разово або тартрату двічі на добу), для якого Т/Р становило щонайменше 70-80% [8, 9, 24];
- високий відсоток пацієнтів літнього віку (у дослідженні ASCOT-BPLA – 84% старше 55 років) при виключенні хворих із достовірною ІХС (перенесений ІМ, стенокардія напруги тощо), що не відповідає структурі загальної популяції [15, 16, 18, 24, 31];
- однаковий вплив атенололу й каптоприлу на прогноз у хворих на АГ та інсуліннезалежний ЦД (UKPDS, 1998) [34] ставить під сумнів гіпотезу про негативну метаболічну дію БАБ як причину їх нібито негативного впливу на кінцеві точки у пацієнтів з АГ [24].
Крім того, прогностичним критерієм високої ефективності БАБ є висока ЧСС у спокої до призначення препарату [1, 11, 16, 24], що не враховується під час рандомізації у трайл. Результати вітчизняного відкритого дослідження ПРОЛОНГЕР-2 (2006) за участю 6000 пацієнтів з АГ, які отримували невисокі дози ретардного метопрололу (більш ніж 70% осіб – 25-50 мг/добу), підтверджують користь навіть помірного зниження ЧСС для досягнення цільових показників АТ [17]. БАБ є препаратами вибору для початкової терапії у хворих, які мають:
- вік до 55 років;
- ІХС (стенокардію напруги і спокою, перенесений ІМ, безбольову ішемію міокарда, що виявляється за допомогою електрокардіограми [ЕКГ]) [1, 11, 12, 40];
- тахікардію, тахіаритмії: часту екстрасистолію, постійну або персистуючу фібриляцію передсердь (для контролю частоти скорочень шлуночків – клас І, рівень доказовості А), особливо на фоні ІХС за відсутності ознак затримки рідини [32];
- ХСН зі зниженою фракцією викиду (ФВ) лівого шлуночка (ЛШ);
- на фоні обструкції вихідного тракту ЛШ – неоперований аортальний стеноз, гіпертрофічну кардіоміопатію;
- гіпертиреоз, глаукому тощо.
У хворих старше 65 років монотерапія БАБ доцільна лише за наявності супутніх показань, зазначених вище [24]; разом із тим БАБ ефективні як додаткові препарати, зокрема у формі фіксованих комбінацій атенололу з діуретиками та антагоністами кальцію задля підвищення комплаєнсу (менше таблеток на добу, низька вартість). Обов’язкова кратність застосування, що забезпечує індекс Т/Р вище 50% – двічі на добу для атенололу і метопрололу тартрату, разово – для бісопрололу та метопрололу сукцинату. За поєднанням комплаєнсу та фармакоекономічних параметрів перевагу має бісопролол (Т/Р>85%, висока селективність), особливо при систолічній ХСН. Після перенесеного ІМ переваги має лікування метопрололом.
Хворим із підвищеним ризиком розвитку ПР (хронічними захворюваннями бронхів, периферичних судин, хронічною нирковою недостатністю тощо) БАБ доцільно призначати лише за наявності додаткових показань або при недостатній ефективності комбінації ЛЗ інших класів; перевагу має лікування бісопрололом починаючи із низьких доз (2,5 мг разово, рідше – 1,25 мг).
Атенолол, з огляду на дані останніх метааналізів, використовувати для монотерапії АГ небажано.
БАБ можуть ефективно купірувати прояви гіпертензивного кризу [2, 12, 32].
При неускладнених гіпертензивних кризах доцільно застосовувати таблетований метопрололу тартрат (краще розжувати) у дозі 25-50 мг, гіпотензивна дія якого розпочинається за 30-45 хв після прийому і триває 8-12 год [2, 11, 12]. Метопролол перевершує традиційний пропранолол за рахунок селективності (нижчий ризик ПР) та кращого комплаєнсу при подальшому призначенні. Є препаратом вибору в лікуванні деяких хворих з АГ (зазначалося вище), а також:
- при гіперкінетичному або симпатоадреналовому гіпертензивному кризі , що характеризується тахікардією, збудженням, швидким (хвилини, години) розвитком на фоні фізичного або нервового напруження. Периферичні вазодилататори можуть посилювати симптоми через рефлекторну симпатичну активацію [2, 4]. У пацієнтів із підозрою на феохромоцитому БАБ слід комбінувати з α-блокаторами (празозин під язик від 1 мг) [7, 11];
- при підозрі на синдром відміни БАБ (див. розділ «Побічні реакції на препарати групи БАБ») після з’ясування режиму антигіпертензивної терапії та його можливих порушень [2];
- у комбінації з ніфедипіном, α-блокаторами перорально, петльовими діуретиками, за наявності ІХС – з нітратами. Потенціюючи дію ЛЗ зазначених класів, БАБ запобігають виникненню їхніх ПР – тахікардії, екстрасистолії, ішемії міокарда, ортостатичної гіпотензії та синдрому «рикошету» – швидкому підвищенню АТ після закінчення дії [2].
При кризі, ускладненому ГКС, тахіаритміями, перевагу надають лабеталолу від 20 мг або метопрололу від 2,5-5 мг внутрішньовенно, у разі їх недоступності – метопрололу перорально.
Протипоказання для застосування БАБ наведені у відповідному розділі, недоцільним воно також видається при гіпертензивному кризі за наявності ознак застою рідини, у разі попереднього прийому ЛЗ із групи БАБ у повній терапевтичній дозі або вживання верапамілу, дилтіазему, а також при підозрі на синдром відміни клонідину (останній є препаратом вибору) [2].
Вираженість антигіпертензивного ефекту метопрололу при гіпертензивному кризі є предиктором ефективності БАБ для подальшої постійної терапії, що скорочує термін досягнення цільового АТ і кількість візитів пацієнта до лікаря.
ІХС: гострий інфаркт міокарда
Починати терапію БАБ потрібно якомога раніше в усіх пацієнтів без протипоказань з метою зниження смертності та ризику рецидиву ІМ (клас І, рівень доказовості А) [1, 32, 40, 41]. За відсутності реперфузії достовірний ефект раннього призначення БАБ виявляється вже на 7-у добу (атенолол у дослідженні ISIS1, 1988) [2, 40]. Доведена ефективність низки препаратів переважно короткої дії (для відміни або корекції дози в разі розвитку гіпотензії або гострої серцевої недостатності), зокрема для атенололу і метопрололу, причому при використанні їх у високих дозах (100 мг/добу – для атенололу, 200 мг/добу – для метопрололу). Внутрішньовенне введення 2,5-5 мг метопрололу повільно (загалом до 15 мг) доцільне для купірування ангінозного болю, особливо за неефективності наркотичних анальгетиків, у разі значно підвищеного АТ (клас І, рівень доказовості В) і при надшлуночкових та шлуночкових аритміях [1, 32, 40]. З урахуванням 1,5-2-годинної затримки контакту хворого з лікарем спеціалізованого відділення вкрай важливим видається надання допомоги у максимально доступному обсязі лікарем первинної ланки. Насамперед вона має включати нітрати сублінгвально, гепарин та анальгетики внутрішньовенно й метопролол перорально (розжувати) у дозі 25-50 мг залежно від показників АТ і ЧСС (перевага над пропранололом завдяки меншій негативній ізотропній дії). Протипоказання – ознаки гострої серцевої недостатності, артеріальна гіпотензія нижче 100 мм рт. ст. або різке зниження АТ у динаміці, брадикардія чи блокади (особливо при задньому ІМ) та виражена бронхообструкція.
ІХС: гострий коронарний синдром
Об’єднує нестабільну стенокардію та ІМ без зубця Q та елевації сегмента SТ. Показання і способи застосування БАБ такі самі, як і при гострому ІМ. Щодо зменшення ішемії і попередження розвитку гострого ІМ – клас І, рівень доказовості В [1, 40].
ІХС: перенесений ІМ
Усі пацієнти за відсутності протипоказань мають постійно застосовувати ЛЗ із групи БАБ (клас І, рівень доказовості А) [1, 7, 41]. Зниження однорічної смертності становить у середньому 20-25%, насамперед за рахунок серцево-судинної (РСС, від повторного ІМ), що відповідає одному врятованому життю на 88 пролікованих протягом року хворих. Позитивний ефект БАБ спостерігається в усіх таких пацієнтів, зокрема із хронічними захворюваннями легень, нирок та ЦД (користь навіть більш виражена) [21], після проведеної реваскуляризації та зберігається щонайменше 5 років.
Зниження смертності не фіксувалося при застосуванні БАБ із внутрішньою симпатоміметичною активністю (за винятком ацебутололу, в якого ця активність є слабкою) і соталолу [2, 6], а для атенололу в дозі 50 мг/добу (ISIS-1, 1988) втрачався до кінця першого року достовірний позитивний ефект [2, 32]. Переваги пропранололу і метопрололу доведено при титруванні доз до субмаксимальних (відповідно 180-240 і 200 мг/добу) [41]. Отже, зниження летальності у хворих після перенесеного ІМ напряму залежить від потужності β-адреноблокади, тобто необхідне титрування дози до досягнення ЧСС 55-60 уд/хв або принаймні до субмаксимальної. Проте застосування БАБ у цієї категорії хворих у світі є недостатнім, причому найменшим – за наявності ЦД (лише 20-30%), коли користь від ЛЗ є більш вираженою [21, 44].
У хворих із гострим ІМ цільова доза БАБ досягається не завжди, зважаючи на скорочення терміну перебування у стаціонарі (неускладнений ІМ – 10-14 діб), коливання АТ, ЧСС, транзиторну серцеву недостатність, наявність ускладнень ІМ (наприклад, АV-блокада ІІ-ІІІ ступеня при великому задньому ІМ), супутніх захворювань (зокрема ЦД) та необхідність призначення ще 2 груп ЛЗ із гіпотензивною дією – ІАПФ та нітратів, а іноді – антиаритмічних препаратів (ААП) ІІІ класу. Тому вкрай важливим видається підвищення доз БАБ до цільових на післягоспітальному етапі або перегляд раніше наявних протипоказань для їх призначення. Можливим є зниження дози або відміна нітратів тривалої дії чи молсидоміну (при відсутності або нечастих нападах стенокардії), діуретиків; мінімізація дози аміодарону (до 100 мг/добу) на фоні титрування дози БАБ. При цьому необхідний контроль АТ, ЧСС та навчання хворого самоконтролю (дії в разі нападу стенокардії, контроль АТ із можливою корекцією доз ЛЗ тощо).
З урахуванням доказової бази та фармакоекономічних параметрів ЛЗ вибору в таких випадках має бути метопролол (триваліша дія та вища селективність порівняно з пропранололом) із доведенням дози до максимально переносимої або 200 мг/добу за 2-3 прийоми для метопрололу тартрату або разово – для сукцинату. У разі зниженої ФВ ЛШ < 45-50%, а також високого ризику ПР можна застосовувати бісопролол (до 10 мг/добу), який має перевагу перед метопрололу сукцинатом за рахунок нижчої вартості. Пацієнт має бути обов’язково попереджений про необхідність постійного застосування ЛЗ із метою зниження ризику ускладнень і смертності та про небезпеку раптового припинення лікування.
ІХС: стабільна стенокардія напруги
БАБ є препаратом першого вибору для контролю ішемії міокарда в усіх хворих без протипоказань (клас І, рівень доказовості А), для профілактики ІМ (клас І, рівень доказовості В) і, можливо, для позитивного впливу на виживання (клас І, рівень доказовості С), чим визначається його перевага над антагоністами кальцію і нітратами тривалої дії [1, 22]. БАБ ефективно знижують тривалість безбольової ішемії міокарда.
Рекомендовано для застосування три препарати – метопрололу сукцинат, атенолол і бісопролол [22, 23]. Протиішемічна активність метопрололу сукцинату в дозі 200 мг 1 раз на добу була достовірно вищою за таку ніфедипіну-ретарду в дозі 20 мг 2 рази на добу, особливо при більшому значенні подвійного добутку (ЧСС, помножена на систолічний АТ) в спокої та на фоні порогового фізичного навантаження, а також при вищому показникові функціонального класу, що було продемонстровано в дослідженні ІМАGE (1995; n=280) [8, 9]. Метопролол сукцинат при спостереженні за 800 хворими протягом 3 років не поступався за впливом на загальну смертність та кількість серцево-судинних подій антагоністу кальцію верапамілу за однакової переносимості обох ЛЗ (APSIS, 1996) [8, 9].
За даними добового моніторування ЕКГ у дослідженні ТІВВS (1996; n=330) бісопролол у дозі 10 мг був ефективнішим за ніфедипін-ретард у дозах 20 і 40 мг 2 рази на добу щодо зменшення кількості нападів стенокардії та епізодів і тривалості ішемії. Хоча подвійні дози ЛЗ достовірно додатково зменшували кількість ангінозних нападів, загальний час ішемії не змінився. Протягом року спостереження частота великих серцево-судинних подій була достовірно нижчою у групі бісопрололу. При цьому чітким маркером ефективності профілактики великих подій було 100% усунення ішемії міокарда за допомогою бісопрололу [2, 16].
Атенолол рекомендовано для використання на основі багатьох невеликих клінічних досліджень, його застосу-вання двічі на добу забезпечує контроль ішемії у ранкові години [22, 32].
Необхідність досягнення високих доз БАБ для лікування стенокардії напруги є ще більш нагальною, ніж при АГ [23]. Для метопрололу цільовою дозою є 200 мг/добу (рекомендованою формою є сукцинат 1 раз на добу [22], проте з огляду на нижчу вартість можливе застосування метопрололу тартрату 2-3 рази на добу по 25-100 мг), бісопрололу – 10 мг/добу, атенололу – 50 мг двічі на добу. В окремих випадках призначають більш високі дози індивідуально для досягнення ЧСС у спокої 50-55 уд/хв.
У разі недостатньої ефективності цільової дози БАБ можливе комбінування з:
- нітрогліцерином для купірування нападів на фоні постійної терапії БАБ;
- дигідропіридинами тривалої дії у субмаксимальних дозах (фелодипін пролонгований 10 мг 1 раз на добу [FEMINA, 1997], амлодипін 10 мг/добу, ніфедипін GITS 30-60 мг/добу), особливо за наявності вазоспастичного компонента (ступінь коронарографічних змін не відповідає тяжкості клінічних проявів) та АГ; протипоказані антагоністи кальцію короткої дії;
- триметазидином по 20 мг тричі на добу, у разі застосування його пролонгованої форми – по 35 мг двічі на добу [2, 22].
Адитивний антиангінальний ефект нітратів тривалої дії не доведений у трайлах.
Не рекомендовано поєднання БАБ з верапамілом або дилтіаземом через підвищений ризик АV-блокади ІІ-ІІІ ступеня. В окремих випадках, коли при максимальній дозі БАБ зберігається стенокардія напруги високого функціонального класу і спокою на фоні високої ЧCC і є неможливою реваскуляризація (з економічних причин або при коронарографічно інтактних артеріях – «синдром Х»), можливе приєднання верапамілу у субтерапевтичній дозі 40 мг тричі на добу під контролем показників АТ, ЧСС та ЕКГ (особливо – довжини інтервалу PQ), за необхідності – показників добового моніторування ЕКГ. Дозу можна збільшити не раніше ніж через 7 днів.
Бісопролол перевершує за комплаєнтністю (застосування разово на добу) атенолол і метопрололу тартрат і за вартістю – метопрололу сукцинат або ретард. Використання метопрололу в дозі 200-300 мг/добу може бути корисним при важко коригованій ішемії, коли не досягається ЧСС 55-60 уд/хв при прийомі бісопрололу у дозі 10 мг.
Хронічна серцева недостатність зі зниженою систолічною функцією ЛШ
Характеризується ФВ ЛШ за даними ехокардіоскопії менше 40-45%. Доведено здатність БАБ покращувати виживання хворих із ХСН ІІ-ІV функціонального класу за NYHA, незалежно від етіології (клас І, рівень доказовості А) [1, 26].
У пацієнтів після перенесеного ІМ БАБ найбільше знижували смертність у групі хворих зі зменшеною ФВ ЛШ (особливо у перші дні після ІМ, навіть у разі її подальшої нормалізації ) [41]. При спостереженні з середньою тривалістю 1 рік 3 місяці зниження смертності на 30-35% відмічено в осіб із ХСН і ФВ ЛШ<35-40% для метопрололу сукцинату (MRIFT-HF, 1999; n=3991) [42], бісопрололу (СІВІS11, 1999; n=2647) [43] та карведилолу (COPERNICUS, 2001; n=2289), що відповідає 28 пролікованим пацієнтам на рік для збереження одного життя. Зазначений ефект досягався за рахунок вираженого зменшення кількості випадків РСС більш ніж на 40% у кожному з досліджень і був зворотно пропорційним ФВ ЛШ (найвищий при ФВ <25%). Критерії терапії БАБ хворих із ФВ ЛШ <35-45%: компенсований стан (усунення ознак затримки рідини), терапія ІАПФ, титрування дози не частіше ніж раз на 7 днів із субтерапевтичної до субмаксимальної (табл. 2).
У трайлі СІВІS ІІ не виявлено різниці у виживанні між групами пацієнтів, які отримували лікування різними дозами бісопрололу (від 2,5 до 10 г/добу) [43], що свідчить про користь призначення навіть невисоких доз БАБ.
Небіволол включено до рекомендацій за результатами дослідження SENIORS (2005; n=2123): у субаналізі показано виражене зниження летальності у підгрупі хворих із ФВ ЛШ <35%. Прийом БАБ не впливає на смертність пацієнтів зі збереженою ФВ ЛШ і симптомами ХСН (за відсутності клапанних вад), незважаючи на негативні іно- та хронотропний ефекти та дію на основні причини діастолічної дисфункції – АГ та ішемію міокарда. Проблема терапії таких хворих залишається актуальною [31]. Результати дослідження BEST (2001; n=2708), у якому неселективний вазодилататорний буциндолол достовірно не знижував смертність протягом дворічного спостереження, свідчать про те, що не всі БАБ без внутрішньої симпатоміметичної активності можуть мати вплив на летальність хворих із систолічною ХСН. Отже, таким пацієнтам не слід призначати ЛЗ без доведеної дії (атенолол, пропранолол тощо).
Разом із тим установлена достовірно нижча (на 17%) смертність при застосуванні карведилолу порівняно з метопрололу тартратом у порівняльному дослідженні СОМЕТ (2003; n=3029) тривалістю 4,8 року [25]. Це, ймовірно, пояснюється недостатньою цільовою дозою метопрололу тартрату (50 мг 2 рази на добу) порівняно з карведилолом (25 мг двічі на добу), що призвело до достовірно меншого ступеня β-адреноблокади у групі метопрололу (менше зниження ЧСС і АТ). Цей факт не дозволяє відмовитися від використання метопрололу тартрату у пацієнтів зі зниженою ФВ ЛШ, зважаючи на його нижчу вартість, особливо після перенесеного ІМ. Водночас видається бажаною поява економічно більш доступного метопрололу сукцинату в дозі 200 мг.
Результати дослідження СІВІS III (2005; n=1010) у хворих зі систолічною ХСН віком старше 65 років засвідчили можливість використання бісопрололу у компенсованих пацієнтів до початку застосування ІАПФ. При звичайному режимі титрування бісопролол (від 1,25 мг до 10 мг разово) демонстрував тенденцію до зниження смертності за рахунок попередження РСС на фоні дещо більшої кількості госпіталізацій, що пояснювали жорсткішою гемодинамічною дією БАБ. Після 6 міс монотерапії в лікування включали другий препарат (еналаприл), який призначали за відповідними схемами титрування. Загалом спостереження тривало 24 міс, упродовж яких указані тенденції зберігалися. Початок терапії з БАБ виявився більш ефективним у пацієнтів із вихідною ФВ ЛШ <28%. Вибування з дослідження через ПР БАБ або ІАПФ достовірно не відрізнялося (близько третини хворих у кожній групі) [27]. Високий відсоток вибування вказує на доцільність уповільнення титрування БАБ та ІАПФ в осіб із вираженою гемодинамічною відповіддю.
Найвищу клінічну користь від застосування БАБ як початкової терапії можна очікувати у хворих із синусовою тахікардією, тахісистолічною фібриляцією передсердь, шлуночковою екстрасистолією тощо. Проте дотепер в Україні лише невелика частина пацієнтів із систолічною ХСН отримують БАБ, цільові дози досягаються вельми рідко через перебільшення лікарями первинної ланки небезпеки ПР БАБ [31].
Повна відміна БАБ, навіть поступова, є небезпечною у пацієнтів із систолічною ХСН: так, у СІВІS ІІ летальність у групі відміни зросла більш ніж удвічі [43]. Тому при виникненні ПР слід намагатися продовжити прийом БАБ у меншій дозі. У разі припинення застосування БАБ через 1-3 дні його поновлюють у тій самій дозі, через 3-7 днів – у половинній, більше 7 днів – розпочинають із мінімальної.
З описаних препаратів найпривабливішим за співвідношенням ціна – якість видається бісопролол. Можливим є використання метопрололу сукцинату, метопрололу тартрат доцільний після перенесеного ІМ та у малозабезпечених пацієнтів.
Аритмії серця
БАБ належать до ІІ класу антиаритмічних препаратів за класифікацією Воген-Вільямса, їхня активність досягається за рахунок гальмування симпатичної активації, скорочення інтервалу QТ [2] і виражена проти переважної більшості надшлуночкових та шлуночкових тахіаритмій. Вона є помірною (у середньому 40-60% ефективності залежно від типу аритмії), поступаючись такій насамперед ААП ІС класу – етацизину, пропафенону тощо (до 80-90% ) та ІІІ класу – аміодарону (близько 70%). До переваг БАБ належать: наявність антиішемічного й антигіпертензивного ефектів (вплив на причини більшості прогностично значущих аритмій); покращання виживаності пацієнтів після ІМ та із систолічною ХСН; відсутність значної проаритмогенної дії та кумуляції.
Доведено безпечність та ефективність комбінацій БАБ з ААП аміодароном (зниження смертності у хворих зі шлуночковими аритміями, особливо при ІХС), із дигоксином для контролю ЧСС при тахісистолічній фібриляції передсердь, ААП ІС класу (протекція аритмогенної дії останніх). Зазначені комбінації особливо актуальні в Україні з огляду на недостатню поширеність електрофізіологічного лікування і встановлення двокамерних стимуляторів та імплантованих кардіовертерів-дефібриляторів пацієнтам високого ризику.
Дослідження за участю хворих після перенесеного ІМ, із систолічною ХСН показали зниження смертності за рахунок РСС на 25-35% за рік у групі БАБ порівняно із контролем [41-43], ймовірно за рахунок їхньої антифібриляторної активності.
В ефективних дозах протиаритмічна активність БАБ без внутрішньої симпатоміметичної активності є подібною. Оскільки протиаритмічний ефект триває менше за негативний хронотропний, ЛЗ необхідно застосовувати з достатньою частотою: разово – для метопрололу сукцинату або ретардного та бісопрололу, двічі – для атенололу і 2-3 рази на добу – для метопрололу тартрату; особам групи високого ризику слід призначати максимально переносимі дози. Перевагами бісопрололу є висока селективність і можливість застосування раз на добу.
Синусова тахікардія. Стійке підвищення ЧСС > 90 уд/хв вимагає пошуку та корекції відповідної причини. БАБ ефективно знижують ЧСС при гіперсимпатикотонії, гіпертиреозі, тривожності, ІХС (перенесений ІМ), систолічній ХСН тощо (клас І, рівень доказовості С), симпатоадреналових гіпертензивних кризах; не показані при гіпертермії, гострих або хронічних запальних процесах. З обережністю БАБ призначають при анемії, недостатності аортального клапана, оскільки тахікардія у цих випадках є компенсаторною.
Надшлуночкова екстрасистолія потребує втручання тільки за наявності симптоматики і погіршання якості життя або якщо є пусковим механізмом пароксизмальної тахікардії, фібриляції чи тріпотіння передсердь. БАБ ефективні для симптоматичного лікування.
Надшлуночкові пароксизмальні тахікардії. Ефективність БАБ для купірування пароксизму порівнянна із такою верапамілу при АV вузловій реципрокній тахікардії (клас І, рівень доказовості С), а при фокусній передсердній тахікардії, зумовленій глікозидною інтоксикацією, БАБ мають переваги (клас ІІ, рівні доказовості А, С), проте вартість їхніх внутрішньовенних форм значно вища. БАБ є високоефективними препаратами для профілактики рецидивів таких аритмій (клас І, рівні доказовості С, В), зокрема в пацієнтів із додатковими шляхами проведення [1].
Фібриляція передсердь. Поширеність у популяції становить 0,5-0,7%. При найчастішому тахісистолічному варіанті БАБ є одним із препаратів вибору як для ургентного зниження ЧСС під час пароксизму (клас І, рівень доказовості А), так і для контролю ЧСС при постійній формі фібриляції передсердь (клас І, рівень доказовості В) [1, 28], перевершуючи за ефективністю дигоксин та аміодарон, хоча кардіоверсія при цьому настає досить нечасто (клас ІІ, рівні доказовості А, В). Залежно від ступеня ургентності перевага надається метопрололу внутрішньовенно (при ішемії міокарда, вираженій АГ) у дозі 5-15 мг або перорально (бажано розжувати) у дозі 25-50 мг, у тому числі перед здійсненням кардіоверсії за допомогою ААП І класу або аміодарону. Протипоказаннями, крім загальних, є декомпенсація ХСН (клас ІІ, рівні доказовості В, С) та фібриляція передсердь у пацієнтів із додатковими шляхами проведення через ризик розвитку фібриляції шлуночків.
Оскільки найвищий рівень доказовості (ІС) у профілактиці нападів фібриляції передсердь має «попередження ситуацій, які провокують напад» [28], БАБ показані більшості хворих із персистуючою фібриляцією передсердь, насамперед за наявності АГ, перенесеного ІМ, систолічної ХСН, після екстракардіальних оперативних втручань та в разі зв’язку пароксизмів із фізичним або психоемоційним напруженням.
Згідно з результатами подвійного сліпого дослідження (2000; n=394), метопролол перевершував плацебо щодо збереження синусового ритму – 60 проти 49% хворих протягом 6 міс спостереження, нижчою була й ЧСС при виникненні пароксизму [2, 8]. Ефективність бісопрололу порівнянна із такою карведилолу та соталолу [2].
БАБ перевершують за безпечністю аміодарон, який при застосуванні навіть незначних доз (100-200 мг/добу) може спричиняти ПР з боку щитоподібної залози, печінки, очей, що вимагає постійного лікарського контролю і повторних біохімічних аналізів, а у дозі 400 мг/добу існує ризик життєво загрозливого фіброзу легень [2-4].
Верапаміл та дилтіазем порівнянні з БАБ за ефективністю, є пріоритетними у лікуванні обструктивних уражень бронхів, периферичних судин тощо, однак мають вищий ризик АV-блокади [2, 5].
Препарати класу ІС ефективніші за БАБ щодо підтримання синусового ритму у хворих без тяжкого структурного ураження серця, особливо при невисокій ЧСС. Доцільно поєднувати їх із невисокими дозами БАБ (або антагоністів кальцію) з метою зменшення проаритмогенної дії та ЧСС шлуночків у разі виникнення пароксизму [2, 28].
Визнана активність БАБ для контролю ЧСС у пацієнтів із постійною фібриляцією передсердь, особливо на фоні фізичного навантаження (за ефективністю переважають дигоксин). За наявності систолічної ХСН після насичення глікозидом та досягнення еуволемії БАБ титрується за звичайною схемою з паралельним зниженням дози дигоксину, з подальшою можливою відміною останнього.
Тріпотіння передсердь – прогностично серйозніше за фібриляцію передсердь через ризик виникнення АV-проведення 1:1 із наступною фібриляцією шлуночків. Лікуванням вибору є надчаста черезстравохідна електрокардіостимуляція або кардіоверсія. БАБ мають доведену ефективність щодо зниження ЧСС шлуночків (клас І, рівень доказовості С) у стабільних хворих. Ефективність БАБ достовірно вища порівняно з аміодароном (за винятком ситуацій, коли у пацієнта наявна ХСН або додаткові шляхи проведення). Для профілактики рецидивів проводять медикаментозну терапію, аналогічну лікуванню при фібриляції передсердь, проте перевагу віддають інвазивним втручанням.
Шлуночкові аритмії. Згідно з результатами дослідження CAST (1989), застосування ААП І класу у післяінфарктних пацієнтів призводило до збільшення смертності, незважаючи на ефективне пригнічення шлуночкової екстрасистолії і шлуночкової тахікардії. У зв’язку з цим зросла роль БАБ як ААП завдяки позитивному впливу на прогноз хворих на ІХС із загрозою фібриляції шлуночків [1, 2, 41].
Загалом, БАБ є ЛЗ вибору в лікуванні шлуночкової екстрасистолії та для профілактики життєво небезпечних шлуночкових аритмій у пацієнтів із різними формами ІХС – ГКС, після перенесеного ІМ, стабільною стенокардією, особливо при ймовірному ішемічному або симпатоадреналовому механізмі аритмій (зв’язок із підвищенням ЧСС, ішемією при фізичному напруженні або у ранкові години за холтерівським моніторуванням ЕКГ). У пацієнтів з ІХС бісопролол ефективно зменшував добову кількість шлуночкових екстрасистолій (на 70%), майже у 75% хворих забезпечував повне усунення пробіжок шлуночкових тахікардій (О.С. Сичов та співавт., 2005; n=64). Хоча дозу бісопрололу можна було титрувати до максимальної – 20 мг/добу, середня ефективна доза становила 3,3 мг/добу. У разі неефективності БАБ та при неішемічній етіології аритмій препаратом вибору є аміодарон, а його комбінація із БАБ поступається лише імплантації кардіовертера-дефібрилятора. За необхідності призначення ААП І класу приєднання низьких доз БАБ нівелює негативний вплив цих ЛЗ на виживання [2].
 Стандарти надання допомоги кардіологічним хворим
Стандарти надання допомоги кардіологічним хворим
 Ефективність застосування інгібітора ГМГ-КоА-редуктази Ловастатину-КМП у хворих на прогресуючу стенокардію
Ефективність застосування інгібітора ГМГ-КоА-редуктази Ловастатину-КМП у хворих на прогресуючу стенокардію
 Цукровий діабет, переддіабет і серцево-судинні захворювання. Аналіз рекомендацій Європейського товариства з кардіології (ESC) і Європейської асоціації з вивчення діабету (EASD)
Цукровий діабет, переддіабет і серцево-судинні захворювання. Аналіз рекомендацій Європейського товариства з кардіології (ESC) і Європейської асоціації з вивчення діабету (EASD)
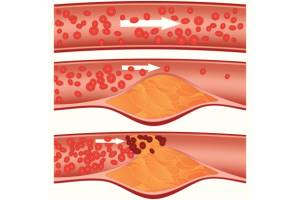 Ішемічна хвороба серця: класифікація, схеми діагностики та лікування
Ішемічна хвороба серця: класифікація, схеми діагностики та лікування
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення
