- Головна
- /
- Статті
- /
- Ендокринологія. Цукровий діабет
- /
- Пошук оптимального засобу для терапії болю при синдромі діабетичної ступні
Пошук оптимального засобу для терапії болю при синдромі діабетичної ступні
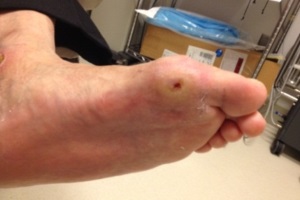
В останні роки ендокринологи, неврологи, лікарі інших спеціалізацій значну увагу приділяють ураженню ніг при цукровому діабеті. Комплекс уражень нижніх кінцівок, який розвивається при цьому захворюванні, отримав назву «синдром діабетичної ступні».
Синдром діабетичної ступні є однією з основних причин інвалідизації та смертності хворих на діабет [22]. У Сполучених Штатах Америки хворим на діабет щорічно виконується близько 50 тис. великих та малих ампутацій, у Німеччині — понад 20 тис.
Значна кількість робіт, присвячених вивченню етіології та патогенезу діабетичної ступні, дозволяє займатися активною профілактикою пізніх стадій цього синдрому та запобігати ампутаціям. Дуже детально вивчені розлади чутливості при діабетичній полінейропатії. Зацікавленість сенсорними порушеннями обумовлена тим, що випадіння чутливості при синдромі діабетичної ступні відбувається паралельно до трофічних порушень. Зниження чутливості на фоні змін живлення периферичних тканин призводить до безболісної травматизації ніг, швидкого розповсюдження інфекційного процесу, розвитку гангрен та обумовлює подальшу необхідність ампутації. Своєчасна адекватна патогенетична терапія відновлює чутливість та поліпшує трофіку кінцівок. При лікуванні відмічається паралелізм у регресі сенсорних та трофічних зрушень, тому відновлення чутливості розглядається не лише як підвищення захисних можливостей організму, але і як свідчення поліпшення метаболізму в кінцівках. Переважна роль нейропатії в розвитку синдрому діабетичної ступні та націленість лікаря-ендокринолога на діагностику та лікування втраченої чутливості у діабетиків відволікає його увагу від проблеми синдрому болю у цих хворих. У більшості наукових робіт по вивченню перебігу синдрому діабетичної ступні цей аспект практично ігнорується. Тому логічним вбачається наступне запитання.
Чому болять ноги при цукровому діабеті?
Відповідь на це запитання розпочнемо з патогенезу синдрому діабетичної ступні. У його генезі провідну роль відіграють два фактори: дистальна периферична нейропатія та ішемія [4]. За переважанням дії того чи іншого чинника синдром діабетичної ступні поділяється на нейропатичну (приблизно у 50% хворих), ішемічну (15% хворих) та нейро-ішемічну форми (35% хворих).
Основними клінічними проявами синдрому діабетичної ступні є наступні розлади.
- Нейропатичного генезу [5, 10]:
- розлади чутливості: симптоми подразнення на ранніх стадіях ураження та симптоми випадіння при тривалому перебігу;
- рухові розлади: сенсорна атаксія, судомний синдром, проксимальна аміотрофія;
- вегетативні та трофічні розлади.
- Ішемічного генезу: переміжна кульгавість.
Больові відчуття супроводжують більшість з наведних варіантів ураження кінцівок. Біль у ногах виникає внаслідок подразнення чутливих волокон; такий біль характеризується відчуттям оніміння, горіння в ногах, часто супроводжується парестезіями, відчуттям оніміння. Демієлінізація крупних рухових волокон призводить до розвитку судом у ногах. Вони виникають переважно в стані спокою та в нічний час і також супроводжуються значним болем, який заважає хворому спати. Трофічні порушення супроводжуються деформацією кісток, зміною анатомічних співвідношень складових опорно-рухового апарату і болем. Периферична ангіопатія з облітерацією судин призводить до розвитку дистальної ішемії, яка проявляється болем, що виникає при ходьбі. Таким чином, і нейропатична і ішемічна форма синдрому діабетичної ступні характеризується наявністю больового синдрому.
Біль — один з найбільш частих проявів різноманітних захворювань — є фактором, який значно погіршує якість життя хворих. Важливим критерієм ефективності терапії більшості хвороб у внутрішній медицині є саме її вплив на динаміку больового синдрому. Синдром діабетичної ступні у хворих на діабет — чи не єдиний приклад практичного ігнорування больового синдрому лікарем та хворим. Цілком логічним вбачається наступне запитання.
Чому не приділяється увага больовому синдрому у хворих з синдромом діабетичної ступні?
Є декілька причин, як з боку лікаря, так і з боку хворого. По-перше, як вже було сказано, лікар акцентований на динаміці сенсорних зрушень. По-друге, у тих роботах, де проводився аналіз динаміки больового синдрому на фоні базисної патогенетичної терапії діабетичної полінейропатії, вказується на значно гірше та повільніше зменшення його інтенсивності в порівнянні з відновленням чутливості. По-третє, більшість хворих сприймають біль як неминучий, і не вірять у реальну можливість його усунення чи значного зменшення. І, нарешті, більшість запропонованих у науково-практичній літературі засобів для лікування больового синдрому в таких хворих мають ряд недоліків і неприйнятні для тривалого використання.
Чому відновлення чутливості при використанні патогенетичної терапії відбувається швидше, ніж зникнення болю?
Патогенетична терапія діабетичної полінейропатії на сьогоднішній день передбачає адекватну цукрознижуючу терапію з підтримкою цільових рівнів глікемії протягом доби, застосування вітамінів групи В та альфа-ліпоєвої кислоти [5, 10, 16]. Проспективні дослідження останніх років довели важливу роль нормалізації вуглеводного обміну в запобіганні розвитку та лікуванні синдрому діабетичної ступні [13-15, 18, 19]. Однак ці ж дослідження показали, що ураження нервів та судин при діабеті відбувається і за умов цілком задовільної компенсації вуглеводного обміну. Це визначило необхідність пошуку препаратів зі специфічною нейропротекторною дією. Найширшого використання набула альфа-ліпоєва кислота, яка суттєво покращує перебіг діабетичної нейропатії і має не лише симптоматичний, а й патогенетичний вплив [3, 8, 11, 22-24]. Саме ліпоєва кислота вбачається як надійний засіб патогенетичного лікування діабетичної нейропатії, який сприяє поновленню структури та функції периферичних нервів.
Чутливі волокна — це дрібні нервові волокна, у той час як рухові — крупні мієлінізовані волокна. Структура дрібних волокон при використанні альфа-ліпоєвої кислоти поновлюється значно швидше, ніж крупних моторних волокон, для повноцінного проведення нервового імпульсу в яких має бути відновлена структурна та функціональна цілісність їх мієлінової оболонки. Саме тому судоми та біль у ногах залишаються у хворого ще протягом тривалого часу після відновлення чутливості. Така ситуація вимагає, з одного боку, пролонгації лікування альфа-ліпоєвою кислотою, а з іншого, — проведення симптоматичної терапії.
Чи маємо ми ефективні засоби симптоматичної терапії?
Для лікування болю при синдромі діабетичної стопи використовують різні засоби, але, на жаль, більшість з них не є придатними для тривалого застосування. Запропоновані наступні.
- Нестероїдні протизапальні засоби. На сьогодні широко застосовуються при лікуванні болю різного генезу. Їх застосування при синдромі діабетичної ступні обмежене недостатньою ефективністю, розвитком гастропатій та негативним впливом на хрящову тканину при тривалому використанні.
- Трамадол — анальгетик центральної дії. До його недоліків відносяться можливість розвитку звикання та значний гепатотоксичний вплив.
- Нервові блокади. Метод є досить складним і неможливим для амбулаторного використання хворим. Застосовується короткочасно при значній інтенсивності болю.
- Капсаіцин — екстракт пекучого перцю. Є дані про сприятливий його вплив на больовий синдром, однак даний препарат в Україні не зареєстрований.
- Клонідин — a2-адренергічний агоніст. Зменшує біль, викликаний симпатичними С-волокнами. Пероральний прийом препарату супроводжується значною кількістю небажаних ефектів. Є повідомлення про можливість місцевого застосування клонідину, але в цьому випадку досить складним є підбір ефективної дози [12].
- Тривалі довенні інфузії інсуліну. Метод також є малопридатним для повсякденного лікування.
- Антидепресанти. Дана група препаратів в останні роки застосовувалася найширше. Проте при застосуванні цих препаратів часто розвиваються дизавтономія та сухість у роті, які можуть бути дуже неприємними для хворого.
- Карбамазепін — ефективний при «стріляючому» болю, але має значні токсичні ефекти, які обмежують його використання.
Таким чином, запропоновані в літературі засоби лікування больового синдрому при діабетичній ступні не є прийнятними для тривалого застосування. У зв’язку з цим ми постійно ведемо пошук препарату, який задовольняв би наші вимоги. Останнім часом ми все ширше використовуємо в лікуванні цього синдрому міорелаксант центральної дії — Мідокалм (толперізону гідрохлорид). Наш вибір обумовлений декількома факторами [7]:
- Мідокалм, як міорелаксант призводить до зменшення тонусу м’язів, усуває судоми та викликаний ними біль.
- Мідокалм структурно подібний до лідокаїну і здатний взаємодіяти з рецепторами до нього. Унаслідок цього зменшується біль, викликаний подразненням чутливих волокон.
- Мідокалму притаманна клонідиноподібна дія, що також сприяє зменшенню інтенсивності больового синдрому.
- Унаслідок розслаблення скелетних м’язів та зменшення тонусу судин Мідокалм сприяє покращенню кровообігу в кінцівках, зменшує ішемію і усуває ішемічний біль та переміжну кульгавість.
З метою вивчення ефективності впливу Мідокалму на перебіг больового синдрому у хворих з діабетичною ступнею ми провели клінічне дослідження.
Мета дослідження. Вивчення клінічної ефективності Мідокалму в лікуванні больового синдрому у хворих з синдромом діабетичної ступні.
Загальна характеристика хворих та методи обстеження
Дослідження проводилися на базі ендокринологічного відділення Полтавської обласної клінічної лікарні ім. М. В. Скліфосовського. Ми обстежили 36 пацієнтів: чоловіків — 29, жінок — 7. На цукровий діабет 1 типу страждали 19 осіб, 2 типу — 17 осіб. Вік хворих на діабет 1 типу становив 37,6±1,4 років, на діабет 2 типу — 56,3±1,6 років. Тривалість діабету була 4,7±0,84 років при діабеті 1 типу, та 5,2±1,13 при діабеті 2 типу.
Хворих поділили на дві групи. Пацієнти контрольної групи (19 хворих) з метою лікування полінейропатії отримували цукрознижуючу терапію, альфа-ліпоєву кислоту (Берлітіон, Еспа-Ліпон) у добовій дозі 600 мг та комплекси вітамінів групи В. Десять днів альфа-ліпоєву кислоту вводили довенно, потім переходили на пероральне застосування. Вітаміни групи В застосовувалися перорально (Неуробекс, Нейровітан). Хворі основної групи додатково отримували Мідокалм перорально в добовій дозі 450 мг, розділеній на три прийоми. Тривалість курсового лікування Мідокалмом становила 10 днів. У кінці цього терміну проводили аналіз динаміки больового синдрому. При відсутності болю прийом Мідокалму припиняли, в інших випадках (зменшення болю або відсутність помітної динаміки) терапію продовжували до зникнення больового синдрому — плюс три-чотири дні.
Для оцінки ефективності лікування в контрольній і дослідній групах проводили аналіз основної неврологічної симптоматики, характерної для діабетичної нейропатії, — зміни чутливості та больового синдрому. Для виключення впливу відмінностей у стані метаболічної компенсації на виразність неврологічної симтоматики протягом терміну спостереження проводили динамічний моніторинг показників глікемії та глюкозурії; при необхідності проводили корекцію цукрознижуючої терапії для підтримки нормоглікемії в обох групах.
Результати та їх обговорення
Більшисть хворих з больовим синдромом скаржилися на тупий тягнучий біль у гомілках та стопах, який турбував їх переважно в нічний час та у спокої (табл.). Цей біль є свідченням ураження дрібних нервових волокон [20, 21]. У п’яти хворих цей біль був інтенсивним. Частим був пекучий біль у стопах, який супроводжувався парестезіями. Значна частина хворих скаржилася на судоми в гомілках і стопах. Тупий тягнучий біль у гомілках та судоми відзначалися у хворих переважно в нічний час та в спокої. Таким чином, у хворих відзначалася різна характеристика больових відчуттів, що пов’язано з переважним ураженням у них тих чи інших типів нервових волокон.
Нормалізація глікемії та застосування альфа-ліпоєвої кислоти в контрольній групі призводили до поліпшення перебігу діабетичної нейропатії. Більшою мірою це стосувалося відновлення чутливості, у той час як больовий синдром піддавався терапії значно важче. Більшість видів чутливості відновлювалися у хворих уже протягом десяти днів довенного введення альфа-ліпоєвої кислоти або через декілька днів після переходу на таблетовану форму (рис. 1). Найгірше поновлювалася вібраційна чутливість.
У той же час на наявність болю в ногах хворі скаржилися на 10-й і, навіть, 40-й день терапії (рис. 2), указуючи при цьому на зменшення інтенсивності больових відчуттів (рис. 3). Терміни зникнення болю були довшими, ніж терміни відновлення чутливості (рис. 4).
Наші дані щодо впливу нормалізації глікемії і використання альфа-ліпоєвої кислоти співвідносяться з результатами інших досліджень. У більшості з них також указується на переважний вплив альфа-ліпоєвої кислоти на сенсорні порушення при діабетичній нейропатії. Згідно з даними цих досліджень, після довенного введення альфа-ліпоєвої кислоти (при тривалості курсу — 10-28 днів) поліпшення чутливості відбувається у 85-95% хворих. Описана динаміка больового синдрому не є настільки переконливою. С. М. Віничук [2] указує на повільну регресію больового синдрому та моторних розладів при використанні Еспа-Ліпону. У дослідженні, проведеному в Українському науково-практичному центрі ендокринної хірургії, трансплантації ендокринних органів та тканин МОЗ України, зниження інтенсивності больового синдрому вдвічі досягали при довенному введенні 1200 мг альфа-ліпоєвої кислоти з подальшим тримісячним пероральним прийомом. При використанні середньотерапевтичних доз інтенсивність больового синдрому практично не змінювалася [6]. Чи не єдине дослідження, де описана позитивна динаміка — робота В. М. Скибуна [9], де 20-денне довенне введення альфа-ліпоєвої кислоти та подальший пероральний прийом протягом місяця призводив до зникнення болю у 90%, а судом у 80% хворих. Слід звернути увагу й на те, що в даному дослідженні розглядали хворих з початковою нейропатією, яким призначалися високі дози альфа-ліпоєвої кислоти.
Таким чином, отримані результати та дані інших дослідників вказують на недостатній вплив патогенетичної терапії діабетичної нейропатії на больовий синдром і визначають доцільність застосування симптоматичних засобів.
Застосування в комплексній терапії Мідокалму сприяло швидкому зникненню болю і судом у більшості хворих (рис. 5). Практично з перших днів терапії зменшувалася інтенсивність больового синдрому (рис. 6), терміни його зникнення були значно коротшими в порівнянні з контролем (рис. 4). У першу чергу це обумовлено міорелаксуючими властивостями Мідокалму і зменшенням спастики литкових м’язів. Однак зменшувалася виразність і інших видів болю. Зменшення інтенсивності тупого ниючого болю в стопах може пояснюватися усуненням гіпертонусу екстензорів стопи при застосуванні Мідокалму. Зменшення ж пекучого болю в стопах, характерного для ураження чутливих волокон, скоріше за все пов’язане з лідокаїноподібною та клонідиноподібною дією Мідокалму.
Крім того, при застосуванні в комплексній терапії Мідокалму швидше, ніж в контрольній групі, відновлювалася вібраційна чутливість (рис. 1). Середні строки відновлення інших видів чутливості не відрізнялися між групами.
Важливою складовою терапевтичного ефекту Мідокалму є покращення кровообігу в кінцівках. Позитивний вплив Мідокалму на перебіг облітеруючих захворювань судин був описаний раніше [1], що дозволило рекомендувати препарат до застосування в ангіології, у тому числі при лікуванні діабетичної ангіопатії нижніх кінцівок. Указується на вірогідне збільшення відстані, яку проходили без болю хворі з переміжною кульгавістю на фоні ІІА та ІІВ стадій ішемії нижніх кінцівок [1]. У нашому дослідженні на фоні терапії Мідокалмом зростали реографічні індекси і вірогідно перевищували показники контрольної групи (рис. 7).
Безпечність та переносимість Мідокалму
Терапія в обох групах задовільно переносилася хворими. У двох хворих відзначалася нудота. У хворого контрольної групи вона була обумовлена метформіном. У хворого дослідної групи нудота з’явилася при прийомі Мідокалму, однак через чотири дні вона минула і не призвела до відміни препарату. На фоні прийому Мідокалму не відзначалося негативних змін вуглеводного та ліпідного обміну, не зростала потреба в гіпоглікемізуючих засобах.
Фармекономіка та комплайєнтність
В умовах сьогодення важливим питанням в оцінці будь-якої терапії, окрім її ефективності та безпечності, є фармакоекономічна привабливість. Враховуючи той факт, що хворі на цукровий діабет несуть значні затрати на системи самоконтролю, засоби лікування діабету і його ускладнень, даний аспект є особливо актуальним та соціально важливим. Застосування Мідокалму не впливає суттєво на вартість лікування, однак дозволяє досягти швидкого ефекту в динаміці больового синдрому і підвищує схильність хворих до проведення патогенетичної терапії. Реально відчувши позитивну динаміку, хворі значно лояльніше відносяться до необхідності тривалого застосування альфа-ліпоєвої кислоти. Проведення адекватної патогенетичної терапії забезпечує відновлення структури нерва і сприяє стабілізації процесу. Таким чином, застосування в комплексній терапії діабетичної нейропатії Мідокалму підвищує схильність хворих до лікування і є доцільним ще й з цієї точки зору.
Висновки
- Синдром діабетичної ступні, окрім сенсорних, моторних та вегетативних зрушень, характеризується больовим синдромом.
- Больовий синдром у хворих синдромом діабетичної стопи має гетерогенний характер та потребує тривалої терапії.
- Зникнення болю при традиційній терапії діабетичної нейропатії відбувається значно повільніше, ніж відновлення чутливості, що потребує призначення симптоматичних засобів.
- Пероральний прийом Мідокалму в дозі 450 мг на добу швидко знижує інтенсивність болю у хворих з нейропатичною формою синдрому діабетичної ступні.
- Мідокалм за рахунок вазодилатуючої дії призводить до поліпшення периферичної гемодинаміки та позитивно впливає на перебіг не лише нейропатичної, а і нейроішемічної форми синдрому діабетичної стопи.
- Мідокалм добре переноситься і не впливає негативно на метаболічні показники у хворих на цукровий діабет.
- Швидке зникнення болю при застосуванні Мідокалму сприяє схильності хворих до проведення комплексної терапії.
Література
- Брискин Б.С., Дибиров М.А., Евсеев Ю.Н. и др. Лечение хронической артериальной недостаточности нижних конечностей мидокалмом у больных пожилого и старческого возраста // B: Мидокалм. Сборник научных статей.: К., 2002. — С1-4.
- Виничук С.М. Терапевтическая эффективность препарата эспа-липон в лечении диабетической нейропатии // Журнал практичного лікаря. — 1999. — 33. — С. 50-52.
- Галстян Г.Р., Анциферов М.Б. Лечение дистальной диабетической полинейропатии // Русский медицинский журнал. — 2000. — №4. — С. 201-203.
- Гурьева И.В., Комелягина Е.Ю., Кузина И.В. Диабетическая периферическая сенсомоторная нейропатия. Патогенез, клиника, диагностика. — Методические рекомендации. Москва, 2000. — 23 с.
- Жукова Л.А., Лебедев Т.Ю., Гуламов А.А. количественная оценка выраженности нейропатии у больных сахарным диабетом, ее пофилактика и лечение. — Москва, 2003. — 24 с.
- Ларін О.С., Савран О.В., Скибун В.М. та співавт. Результати лікування діабетичної полінейропатії нижніх кінцівок у хворих на цукровий діабет // Клінічна ендокринологія та ендокринна хірургія. — 2003. — №2. — С. 31-35.
- Мидокалм. Миорелаксант центрального действия (пособие для лечащего врача).: К., 1998. — 12 с.
- Науменко В.Г. Берлитион в лечении диабетической нейропатии // Укр. мед. часопис. — 1999. — №6. — С. 98-102.
- Скибун В.Н. Лечебный эффект эспа-липона в терапии диабетической стопы // Ліки. — 1998. — №2. — С. 89-92.
- Тронько М.Д., Єфімов А.С., Савран О.В. та співавт. Діагностика та лікування синдрому діабетичної стопи. Методичні рекомендації. — К., 2002. — 20 с.
- Тронько Н.Д., Науменко В.Г. Современное лечение диабетической нейропатии.: К., 2000. — 16 с.
- Bays-Smith M.G., Max M.B., Muir J., Kingman A. Transdermal clonidine compared to placebo in painful diabetic neuropathy using a two-stage «enriched enrollment» design // Pain. — 1995. — Vol. 60. — P. 267-274.
- DCCT Research Group. The absence of a glycemic threshold for the development of long-term complications: the perspective of the Diabetes Control and Complications Trial // Diabetes 1996. — Vol. 45. — P. 1289-1298.
- DCCT Research Group. The effect of intensive diabetes therapy on the development and progression of neuropathy // Ann. Intern. Med. — 1995. — Vol. 122. — P. 561-568.
- DCCT Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications of insulin-dependent diabetes mellitus // N. Engl. J. Med. — 1993. — Vol. 329. — P. 977-986.
- Fels G. Tolperisone: Evaluation of the lidocain-like activity by molecular modeling // Arch. Pharm. Med. Chem. — 1996. — Vol. 329. — P. 171-178.
- Green D.A. Prevention and treatment of neuropathy // Pharmacology of diabetes: present practice and future perspectives / Eds. Mogensen C.E., Standl E. — Berlin — New-York: de Gruyter, 1991. — P. 297-324.
- UKPDS Group. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34) // Lancet. — 1998. — Vol. 352. — P. 854-865.
- UKPDS Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in type 2 diabetes (UKPDS 33) // Lancet. — 1998. — Vol. 352. — P. 837-853.
- Vinic A.I., Park T.S., Stransberry K.B., Pittenger G.L. Diabetic neuropathies // Diabetologia. — 2000. — Vol. 43. — P. 957-973.
- Vinic A. Diabetic neuropathy: pathogenesis and therapy // Am. J. Med. — 1999. — Vol. 107. — P. 17S-26S.
- Ziegler D., Gries FA., Spuler M. et al. The epidemiology of diabetic neuropathy // Diabetic Medicine. — 1993. — Vol. 10, Suppl. 2. — P. 82S-86S.
- Ziegler D., Hanefeld M., Ruchau KJ. et al. (ALADIN Study group). Treatment of symptomatic diabetic peripheral neuropathy with the antioxidant ?-lipoic acid // Diabetologia. — 1995. — Vol. 38. — P. 1425-1433.
- Ziegler D., Hanefeld M., Ruchau KJ. et al. Treatment of symptomatic diabetic polyneuropathy with the antioxidant ?-lipoic acid: a 7-month multicenter randomized controlled trial (ALADIN III Study). ALADIN III Study Group. Alpha-lipoic acid in diabetic neuropathy // Diabetes Care 22. — P. 1296-1301.
 Использование Кардоната в комплексном лечении диабетической полинейропатии
Использование Кардоната в комплексном лечении диабетической полинейропатии
 Перспективы использования препарата Диротон у больных артериальной гипертензией и сахарным диабетом 2 типа с микроальбуминурией
Перспективы использования препарата Диротон у больных артериальной гипертензией и сахарным диабетом 2 типа с микроальбуминурией
 Контроль гликемии во врачебной практике
Контроль гликемии во врачебной практике
 Перспективы лечения и профилактики неалкогольного стеатогепатита
Перспективы лечения и профилактики неалкогольного стеатогепатита
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення
