Цимевен® инструкция, аналоги и состав
Загальна характеристика:
міжнародна та хімічна назви: ганцикловір (9-(1,3-дигідрокси-2-пропоксиметил) гуанін);
основні фізико-хімічні властивості: ліофілізат (тверда речовина) білого або майже білого кольору;
склад: 1 флакон містить 546 мг ганцикловіру натрію, що еквівалентно 500 мг вільної активної речовини ганцикловіру;
Форма випуску. Ліофілізат для приготування розчину для інфузій.
Фармакотерапевтична група. Противірусні засоби для системного застосування.
Код АТС J05AB06.
Фармакологічні властивості.
Фармакодинаміка. Ганцикловір – синтетичний нуклеозидний аналог гуаніну, що пригнічує реплікацію вірусів герпесу як in vitro, так і in vivo. До ганцикловіру чутливі такі віруси людини, як цитомегаловірус (ЦМВ), віруси простого герпесу типів 1 і 2 (HSV-1 і HSV-2), вірус Епштейна-Барр і вірус Varicella zoster. Клінічні дослідження обмежувалися оцінкою ефективності препарату у хворих на ЦМВ-інфекцію.
У клітині ганцикловір фосфорилюється клітинною деоксигуанозинкіназою до ганцикловіру монофосфату. Наступне фосфорилювання здійснюється за допомогою декількох клітинних кіназ з утворенням ганцикловіру трифосфату. У клітинах, інфікованих ЦМВ, концентрації клітинних кіназ і ганцикловіру трифосфату підвищені приблизно у 10 разів. Таким чином, в уражених вірусом клітинах відбувається посилене фосфорилювання ганцикловіру. У цих клітинах ганцикловір трифосфат повільно метаболізується, причому 50 - 70% його залишається через 18 год після елімінації ганцикловіру з позаклітинної рідини. Противірусна активність ганцикловіру пояснюється пригніченням синтезу ДНК вірусу за допомогою конкурентного гальмування вбудовування деоксигуанозину трифосфату в ДНК-полімеразу. Це означає, що включення ганцикловіру трифосфату в ДНК вірусу викликає припинення синтезу або дуже обмежує подовження ДНК вірусу.
Фармакокінетика.
У хворих з нормальною функцією нирок період напіввиведення ганцикловіру з плазми після внутрішньовенної інфузії в дозі 5 мг/кг становить, у середньому, 2,9 год із середнім системним кліренсом 3.64 мл/хв/кг. Введення дози 5 мг/кг 2 рази на добу протягом 14 днів не призводило до кумуляції активної речовини у плазмі. Як наведено нижче, порушення ниркової функції призводить до зміни фармакокінетики ганцикловіру.
Креатинін сироватки, Системний плазмовий Період напіввиведення мкмоль/л кліренс, мл/хв/кг з плазми, год
<124 3.64 2.9 125-225 2.00 5.3 226-398 1.11 9.7 >398 0.33 28.5
Показання для застосування. Цитомегаловірусний ретиніт, генералізована цитомегаловірусна інфекція у хворих на СНІД, клінічно виражена цитомегаловірусна інфекція у хворих з імуносупресією.
Цитомегаловірусний коліт, езофагіт, пневмонія, інші ураження внутрішніх органів. Профілактика цитомегаловірусної інфекції після трансплантації органів, на фоні протипухлинної хіміотерапії, у хворих на СНІД.
Спосіб застосування та дози. Розчин, отриманий шляхом розведення стерильного порошку Цимевену, призначений виключно для внутрішньовенного введення.
Не можна перевищувати рекомендовані дози, частоту або швидкість інфузії.
Початкове лікування: інфузія 5 мг/кг із постійною швидкістю протягом 1 год 2 рази на добу (кожні 12 год) (10 мг/кг/добу) протягом 14 - 21 дня у хворих з нормальною функцією нирок.
Підтримуюче лікування: хворим з ослабленою імунною системою, у яких існує небезпека рецидиву цитомегаловірусного ретиніту, можна призначати курс підтримуючого лікування. Рекомендована добова доза становить 6 мг/кг маси тіла 5 разів на тиждень або по 5 мг/кг щодня.
Лікування прогресуючого захворювання: хворим на СНІД може бути потрібно лікування невизначеної тривалості, але навіть при постійному підтримуючому лікуванні ретиніт у таких хворих може прогресувати. Хворим із ретинітом, що прогресує в ході підтримуючого лікування або внаслідок відміни препарату, можна провести повторний курс лікування з режимом дозування початкового лікування.
Хворим із нирковою недостатністю дози варто коригувати у такий спосіб:
Креатинін Доза, мг/кг Інтервал сироватки, мкмоль/л між введеннями (год)
< 124 5.0 12 125-225 2.5 12 226-398 2.5 24 > 398 1.25 24
Шлях введення. Увага! Внутрішньом’язова або підшкірна ін’єкція може викликати сильне подразнення тканин внаслідок високого рН розчину ганцикловіру.
Слід уникати швидкої або болюсної внутрішньовенної ін’єкції, оскільки надлишкові концентрації ганцикловіру у плазмі можуть посилити його токсичність.
Розчинення вмісту флакона. Для приготування інфузійного розчину необхідно розчинити вміст флакона. У кожний флакон (еквівалент, що містить 500 мг ганцикловіру) слід додати 10 мл води для ін’єкцій. Не можна використовувати бактеріостатичну воду для ін’єкцій, що містить парагідроксибензоати, оскільки вони не сумісні із стерильним порошком ганцикловіру і можуть викликати випадання осаду.
При розчиненні вмісту флакона слід дотримуватись обережності. Цю операцію рекомендується робити в поліетиленових рукавичках і захисних окулярах, щоб уникнути контакту із вмістом флакона у разі його ушкодження. При потраплянні розчину на шкіру або слизові оболонки їх варто старанно промити водою з милом. Очі слід промивати чистою водою не менше 15 хвилин.
Для розчинення препарату флакон потрібно струсити. Розчин слід оглянути для виявлення механічних домішок.
Приготування і застосування інфузійного розчину. Із флакона (концентрація ганцикловіру 50 мг/мл) відбирається потрібний об’єм, розрахований виходячи з маси тіла хворого і медичного показання, і додається до відповідної інфузійної рідини (частіше 100 мл) для вливання протягом 1 год. Не рекомендується використовувати інфузійні розчини з концентрацією вище 10 мг/мл. З ганцикловіром сумісні такі інфузійні рідини: простий фізіологічний розчин; 5% розчин декстрози у воді; розчин Рінгера (хлорид натрію, хлорид калію і хлорид кальцію у воді для ін’єкцій); розчин Рінгера-лактату (хлорид кальцію, хлорид калію, хлорид і лактат натрію у воді для ін’єкцій).
Оскільки потрібно застосовувати розчини, які не є бактеріостатичними, всі інфузійні розчини, які містять ганцикловір, повинні бути використані не пізніше ніж через 24 год з моменту розведення, щоб зменшити небезпеку бактеріального зараження. Інфузійний розчин слід зберігати в холодильнику, але не більш 24 год. Не рекомендується його заморожувати.
Побічна дія.
Система крові: Еозинофілія, нейтропенія (38%), тромбоцитопенія (19%).
Лабораторні дослідження. Із-за великої частоти нейтропенії або лейкопенії у хворих, які отримують Цимевен, рекомендується кожні 2 дні протягом перших 14 днів лікування ганцикловіром визначати число лейкоцитів. У хворих, у яких ганцикловір у минулому викликав лейкопенію, а також у хворих з початковим числом лейкоцитів менше 2000 в 1 мкл, його визначення слід проводити щодня.
Загальні: озноб, набряки, інфекції, нездужання.
Судинні: аритмії, артеріальна гіпертензія і гіпотензія.
Центральна нервова система: парадоксальні думки або сновидіння, атаксія, кома, сплутаність свідомості, запаморочення, головний біль, знервованість, парестезії, психоз, сонливість, тремор, судоми. В цілому, неврологічні явища відзначаються в 5% хворих.
Система травлення: нудота, блювання, анорексія, діарея, кровотечі, біль.
Відхилення лабораторних показників: зниження рівня глюкози в крові.
Дихальна система: задишка.
Шкіра і її деривати: алопеція, свербіж, кропив’янка.
Органи чуття: відшарування сітківки у хворих на СНІД з ЦМВ-ретинітом.
Сечостатевий тракт: гематурія, підвищення креатиніну сироватки, підвищення азоту сечовини в крові.
Реакції в місці ін’єкції: запалення, біль, флебіт.
Дані досліджень на тваринах показують, що можливою побічною дією є пригнічення сперматогенезу, зворотне при низьких дозах і необоротне при високих. Клінічних даних щодо цієї побічної дії поки що не отримано. Вважається ймовірним, що внутрішньовенне введення Цимевену в рекомендованих дозах буде призводити до зворотного або стійкого пригнічення сперматогенезу. Результати досліджень на тваринах також вказують на можливість стійкого пригнічення фертильності у жінок. Чоловікам і жінкам дітородного віку слід рекомендувати використовувати ефективну контрацепцію під час лікування Цимевеном. Чоловікам варто порадити користуватися бар’єрним методом контрацепції протягом 90 днів після закінчення лікування.
Експериментальні дослідження показали, що Цимевен викликає точкові і хромосомні мутації в клітинах ссавців in vitro та in vivo. Цимевен слід вважати потенційним канцерогеном.
Протипоказання. Цимевен протипоказаний в період вагітності та годування груддю, у хворих з підозрюваною або відомою підвищеною чутливістю до ганцикловіру або ацикловіру.
Цимевен не призначають хворим із числом нейтрофілів менше 500 в 1 мкл, дітям віком до 12 років.
Передозування. Оборотна нейтропенія. Для швидкого зниження рівня ганцикловіру можна застосовувати гемодіаліз.
Особливості застосування.
Приблизно в 40% хворих, які лікуються Цимевеном внутрішньовенно, розвивається нейтропенія (число нейтрофілів менше 1000 в 1 мкл). Тому Цимевен слід з обережністю застосовувати у хворих із вже наявними цитопеніями або з цитопенічними реакціями на інші препарати в анамнезі, а також в осіб, які в минулому були опромінені або отримували препарати і хімічні речовини з мієлосупресивною дією. Цимевен не слід призначати, якщо число нейтрофілів падає нижче 500 в 1 мкл. Нейтропенія частіше виникає протягом першого або другого тижня індукційної терапії і до досягнення сумарної дози 200 мг/кг. Число нейтрофілів звичайно нормалізується протягом 2 – 5 днів після відміни препарату або зменшення дози.
Тромбоцитопенія (число тромбоцитів менше 50.000 в 1 мкл) спостерігалася в 20% хворих, які отримували Цимевен. Зниження числа тромбоцитів частіше спостерігалося у хворих з ятрогенною імуносупресією після лікування імунодепресантами, ніж у хворих на СНІД. Хворі з числом тромбоцитів менше 100.000 в 1 мкл також мають підвищений ризик даної токсичної дії ганцикловіру.
Застосування у хворих на ниркову недостатність
У хворих з порушенням функції нирок Цимевен слід застосовувати з обережністю. У хворих із зниженим кліренсом креатиніну може спостерігатися збільшення як періоду напіввиведення ганцикловіру, так і його максимальної концентрації у плазмі. У невеликої кількості хворих, які проходили гемодіаліз, рівень ганцикловіру в плазмі після нього знижувався приблизно на 50%.
Призначення Цимевену шляхом внутрішньовенної інфузії повинно супроводжуватися достатнім надходженням води в організм, оскільки ганцикловір виводиться через нирки і нормальний кліренс залежить від адекватної функції нирок. Якщо ниркова функція скомпрометована, потрібно провести корекцію дози.
Високі дози або велика швидкість введення можуть призвести до підвищеної токсичності, тому слід дотримуватися вказівок даної інструкції.
Необхідно уникати потрапляння препарату на шкіру і слизові оболонки.
Розчини Цимевену мають високий рН (9-11) і можуть викликати флебіт і/або біль в місці внутрішньовенної інфузії. Потрібно стежити за тим, щоб ганцикловір вводився лише у вени з достатнім кровотоком, що забезпечує швидке розведення і розподіл препарату.
Хворим на час лікування Цимевеном необхідно застосовувати надійні контрацептиви, а чоловікам ще протягом 3 місяців після закінчення лікування.
Застосування у хворих похилого віку. Дослідження щодо оцінки ефективності або безпеки застосування препарату у хворих похилого віку не проводилися. Оскільки у них часто спостерігається погіршення функції нирок, при призначенні Цимевену цим хворим слід обов’язково враховувати їх стан.
Застосування у дітей. Клінічний досвід лікування цитомегаловірусних інфекцій Цимевеном у хворих віком до 12 років обмежений. Побічні явища, які спостерігалися у цій групі, мало відрізнялися від таких у дорослих хворих. Проте застосування Цимевену у дітей потребує винятково ретельного розгляду через можливість віддаленої канцерогенності і токсичного впливу на репродуктивну функцію.
Призначати препарат дітям можливо лише після ретельного обстеження і лише у тому випадку, коли, на думку лікаря, можлива користь від лікування перевищує цей дуже істотний ризик. Цимевен не показаний для лікування уродженої або неонатальної цитомегаловірусної інфекції.
Вплив на здатність керувати автомобілем і працювати з механізмами
У пацієнтів, які отримують Цимевен, можуть спостерігатися судоми, сонливість, запаморочення, атаксія, сплутаність свідомості і/або кома. У такому разі під час лікування препаратом слід уникати керування автотранспортом та роботи з потенційно небезпечними механізмами.
Взаємодія з іншими лікарськими засобами. Ступінь зв’язування ганцикловіру з білками плазми становить всього 1 – 2%, тому взаємодій, пов’язаних із витісненням із місць зв’язку з білками, очікувати не слід. Можливо, що пробенецид, а також інші лікарські засоби, які знижують канальцеву секрецію або реабсорбцію в нирках, можуть зменшувати нирковий кліренс ганцикловіру і збільшувати період його напіввиведення. Можливо також, що препарати, які пригнічують реплікацію клітинних популяцій, що швидко діляться, таких, як кістковий мозок, сперматогонії і паросткові шари шкіри і слизової оболонки шлунково-кишкового тракту, можуть викликати адитивні токсичні реакції, якщо вони застосовуються одночасно з Цимевеном, а також до або після нього. Через можливість адитивної токсичності при одночасному застосуванні таких препаратів, як дапсон, пентамідин, флуоцитозин, вінкристин, вінбластин, адріаміцин, амфотерицин У, комбінації триметоприму із сульфаніламідами або інших нуклеозидних аналогів, поєднання їх із Цимевеном припустимо лише у тих випадках, коли потенційна користь перевищує можливий ризик. Можливо, що хворі на СНІД одержують або одержували в минулому зидовудин. Оскільки і зидовудин, і Цимевен можуть викликати нейтропенію, не рекомендується призначати їх одночасно під час початкового лікування ганцикловіром. Якщо хворого переводять на підтримуюче лікування Цимевеном, лікар може на свій розсуд знов призначити зидовудин. Отримані дотепер дані щодо невеликої кількості хворих свідчать про те, що в більшості з них підтримуюча терапія ганцикловіром у поєднанні з зидовудином у рекомендованих дозах викликала тяжку нейтропенію.
У хворих, які отримували одночасно Цимевен та іміпенем/циластатин, спостерігалися генералізовані судоми. Ці препарати слід призначати в комбінації з Цимевеном лише після ретельної оцінки існуючого ризику.
Мікофенолат: на підставі результатів вивчення введення разової дози щодо рекомендованих доз ганцикловіру внутрішньовенно та мікофенолату перорально і ефектів погіршення функції нирок на фармакокінетику ганцикловіру та мікофенолату, очікується, що сумісне призначення цих препаратів (які є конкурентами щодо впливу на механізми ниркової канальцевої секреції) буде мати результатом підвищення концентрацій ганцикловіру та MPAG (що є неактивним метаболітом мікофенолату). Пацієнтам з погіршеною функцією нирок, яким призначені ганцикловір та мікофенолат сумісно, повинна бути застосована лише рекомендована доза ганцикловіру; також слід ретельно обстежувати таких пацієнтів. Значних змін у фармакокінетиці MPA (що є активним метаболітом мікофенолату) немає, тому коригувати дозу мікофенолату не потрібно.
Умови та термін зберігання. Зберігати у недоступному для дітей місці при температурі не вище 30°С. Термін придатності - 3 роки.



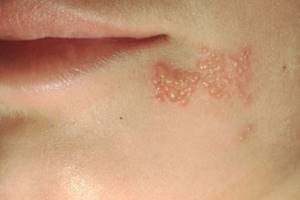 Простий герпес: патогенез, клініка та лікування
Простий герпес: патогенез, клініка та лікування
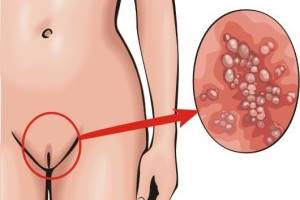 Генітальний герпес: клінічні рекомендації CDC 2006 р.
Генітальний герпес: клінічні рекомендації CDC 2006 р.
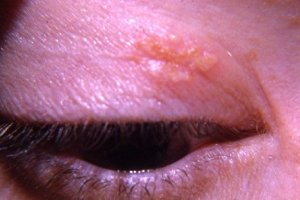 Комплексная терапия больных офтальмогерпесом
Комплексная терапия больных офтальмогерпесом
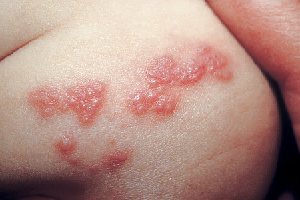 Новый препарат для лечения герпетических кератитов
Новый препарат для лечения герпетических кератитов