- Головна
- /
- Статті
- /
- Гепатологія
- /
- Оцінка ефективності Симепару у хворих на патологію печінки
Оцінка ефективності Симепару у хворих на патологію печінки
Силімарин та його похідні ще з давніх часів застосовують як гепатопротектори. Гастроентерологи та терапевти широко використовують ці засоби у повсякденній практиці, адже поширення патології печінки в усьому світі набирає обертів. За останні роки значно збільшилася поширеність таких основних її нозологічних форм, як гепатит, гепатоз та цироз. Цироз разом із захворюваннями серцево-судинної системи виходить на одне з перших місць серед причин смертності. Отже, ефективне лікування цих захворювань та подовження життя таких хворих є надзвичайно актуальними.
Силімарин (один із найбільш вивчених серед 4 тис. відомих біофлавоноїдів, що має насамперед гепатопротекторний ефект) екстраговано з насіння та плодів рослини Silybum marianum (розторопші плямистої). Це суміш із трьох структурних компонентів: силібініну, силідіаніну та силікристину, хімічну формулу яких було з’ясовано в 60-х рр. ХХ сторіччя. З трьох ізомерів найактивнішою субстанцією є силібінін, що має цитопротекторний та гепатопротекторний ефекти.
Силімарин рекомендується при дегенеративних змінах печінкових клітин, некрозі печінки та її функціональних розладах.
Фармакодинамічні ефекти силімарину
Доведено антагоністичну та захисну дію силімарину проти отруєння фалоїдином, галактозаміном, тіоацетамідом, галотаном, чотирихлористим вуглецем, а також захисну дію від уражень печінки, спричинених ішемією, радіацією, перевантаженням залізом та вірусним ураженням.
Антиоксидантна дія полягає у збільшенні кисневого постачання, зниженні утворення ліпідних пероксидів, підвищенні синтезу сечовини. Оксидативний стрес – структурне та/або функціональне ураження внаслідок неконтрольованого утворення прооксидантних вільних радикалів, дії хімічних речовин, зокрема чотирихлористим вуглецем, етанолу, парацетамолу, фенілгідразину, еритроміцину, амітриптиліну, тетрабутилгідропероксиду. Одним із важливих компонентів захисту є система глутатіону.
У низці досліджень доведено, що лікування силімарином чи силібініном при внутрішньовенному введенні підвищувало вміст глутатіону в печінці, кишечнику і шлунку без підвищення у легенях та нирках. В інших дослідженнях показано, що при дії хімічних оксидантів зменшувалось споживання кисню без змін рівня глутатіону. Силімарин та силібінін послаблюють підвищення аланінамінотрансферази (АЛТ), аспартатамінотрансферази (АСТ), гамма-глутамілтранспептидази (ГГТП) після інтоксикації етанолом чи парацетамолом. Силімарин захищає від дії подібних агентів клітини не лише печінки, а й крові, підвищуючи їх осморезистентність.
Перекисне окислення ліпідів (ПОЛ) – результат взаємодії між вільними радикалами та ненасиченими жирними кислотами жирів. ПОЛ спричинює широкий спектр уражень, призводить до дегенеративних ушкоджень клітинних мембран та подальших розладів ліпопротеїнового метаболізму як у печінці, так і в периферичних тканинах. Силімарин діє за рахунок не лише зниження вільних радикалів, а й активації системи глутатіону та супероксиддисмутази.
При дії етанолу чи галактозаміну силімарин нейтралізує негативний вплив на інгібування синтезу фосфоліпідів, стимулює синтез фосфатидилхоліну, може також знижувати синтез тригліцеридів як у нормальному стані, так і при дії токсичних агентів. Крім того, є дані, що силімарин знижує рівні холестерину та ліпопротеїдів низької щільності при дисліпідемії.
Крім власне захисних ефектів, силімарин проявляє й інші важливі ефекти. Одним із механізмів дії силімарину є стимуляція регенераторних процесів у печінці. Силімарин підсилює формування рибосом та синтез ДНК, що зумовлює підвищення синтезу білка. Цей ефект спостерігається лише в разі ураження печінки і відсутній за нормального фізіологічного стану.
Протизапальний ефект силімарину опосередковується інгібуванням міграції нейтрофілів, купферівських клітин, синтезу лейкотриєнів та утворенням простагландинів. Антиканцерогенний ефект силімарину було вивчено на багатьох тваринних експериментальних моделях.
Насамкінець, силімарин чинить антифібротичну дію за рахунок пригнічення проліферації зірчастих клітин та їх трансформації у міофібробласти.
Силімарин може інгібувати систему цитохрому Р450, хоча не всі дослідники виявили подібні ефекти. Цей ефект може відігравати позитивну роль при інтоксикації, яка опосередкована системою цитохрому Р450, що обмежує токсичність агенту. За таких умов силімарин разом з іншими антиоксидантами захищає від вільних радикалів, що продукуються ферментами цитохрому Р450.
Усі описані ефекти мають складні, до кінця не вивчені клітинні молекулярні механізми, які сьогодні активно досліджуються. Ці ефекти є дозозалежними, отже, для досягнення ефекту рекомендуються тривалі курси з адекватними дозами силiмарину.
Метою нашого дослідження була оцінка ефективності препарату силімарину в лікуванні різних патологій печінки. Ми застосовували препарат Симепар фірми Меpha, що містить 70 мг силімарину та вітаміни, переважно групи В: тіамін (В1) – 4 мг, рибофлавін (В2) – 4 мг, нікотинамід – 12 мг, піридоксин (В6) – 4 мг, кальцію пантотенат – 8 мг, ціанокобаламін (В12) – 1,2 мкг. Додавання вітамінів групи В дає змогу поліпшити функціонування нервової системи, процеси декарбоксилювання та переамінування амінокислот (В6), транспорт водню та утворення АТФ у мітохондріях (В2), нормалізувати окислювально-відновлювальні процеси (нікотинамід), синтез ацетилхоліну, кортикостероїдів, процес регенерації (кальцію пантотенат – В5) тощо.
Під нашим наглядом перебувало 26 хворих на патологію печінки, у 5 з яких було діагностовано неалкогольний стеатогепатит, у 13 – хронічний вірусний гепатит, у 4 – алкогольну хворобу печінки, хронічний гепатит, у 4 – цироз печінки.
Критерії включення хворих у дослідження:
- вік хворих – 18-65 років;
- наявність підтвердженої хронічної патології печінки;
- печінково-клітинна недостатність I-II ст.;
- синдром цитолізу;
- відсутність прийому препаратів силімарину чи есенціальних фосфоліпідів протягом попередніх 6 міс;
- відсутність противірусної терапії;
- відсутність жовчнокам’яної хвороби;
- відсутність клінічно значущої супутньої патології інших органів і систем.
Було проведено базисну терапію: УДХК у дозі 500 мг 1 раз на добу ввечері; лактулоза 10 мл 1 раз на добу ввечері; сорбент атоксил та парентеральна дезінтоксикаційна терапія.
Препарат Симепар призначався в дозі 1 капсула тричі на добу з контролем показників через два тижні. Взагалі препарат рекомендовано для прийому протягом 6 міс.
Оцінка ефективності проводилася за основними клініко-лабораторними показниками: астеновегетативним, больовим, диспепсичним синдромами (оцінювались за бальною системою: 3 – виражений, 2 – помірний, 1 – незначний, 0 – відсутній), симптомами цитолізу та печінково-клітинної недостатності.
До лікування в усіх хворих визначався астеновегетативний синдром різної вираженості. Хворі скаржилися на втомлюваність, слабкість, головний біль, зниження працездатності. Диспепсичний синдром було представлено нудотою натще та після їди, рідко – блюванням, порушеннями випорожнень (проноси, відрижки, здуття, метеоризм). Болі, як правило, локалізувалися в правому підребер’ї і були пов’язані з супутньою біліарною дисфункцією. У всіх хворих на тлі лікування відзначено позитивну динаміку (рис.).
Найважливішою була динаміка синдрому цитолізу, наявність якого була критерієм включення хворих у дослідження.
До лікування середній рівень АЛТ становив 2,27±0,2 ммоль/л, АСТ 0,91±0,3 моль/л, після лікування – АЛТ 1,82±0,12 ммоль/л (р<0,05), АСТ 0,78±0,14 моль/л (р>0,05). Отже, на тлі проведеної терапії у хворих спостерігалася тенденція до зниження рівня трансаміназ. Достовірне зниження АЛТ свідчить про зменшення саме запального цитолізу. Після лікування нормальні показники АЛТ зареєстровано у 12 хворих (38,5%): 4 – на неалкогольний стеатогепатит, 4 – на хронічний вірусний гепатит, 3 – на алкогольну хворобу печінки, хронічний гепатит, 1 – на цироз печінки. У 11 (42,3%) пацієнтів цитоліз зменшився, але не нормалізувався, у 2 (19,2%) – залишився без змін. Отже, можна зробити припущення про гепатопротекторний ефект Симепару. Результати нашого дослідження узгоджуються з відомими даними інших дослідників.
Синдром печінково-клітинної недостатності також зменшувався, достовірно знизився рівень білірубіну – з 29,8±3,8 мкмоль/л до 19,4±2,4 мкмоль/л. Проте, зважаючи на те що хворі отримували інтенсивну дезінтоксикаційну терапію, не проводити яку не етично, оцінити вплив досліджуваного засобу на змiну показникiв бiлiрубину важко.
Побічних ефектів від застосування Симепару не зафіксовано, переносимість була доброю, що також збігається з даними літератури.
На тлі призначення Симепару у складi комбiнованої терапії до 3-го тижня відбулося клiнiчнo значуще зниження АЛТ та поліпшення за всiма клiнiчними симптомами. Ефективність і безпечність такої терапії підтверджуються не лише результатами численних досліджень, але й тривалим застосуванням у клінічній практиці.
Список літератури знаходиться в редакції.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення

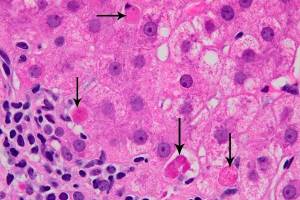 Хронические вирусные гепатиты: проблемы и решения
Хронические вирусные гепатиты: проблемы и решения
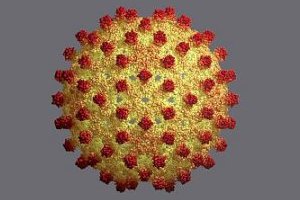 Особенности вирусных гепатитов А и В на современном этапе
Особенности вирусных гепатитов А и В на современном этапе
 Гепатит В и его последствия
Гепатит В и его последствия
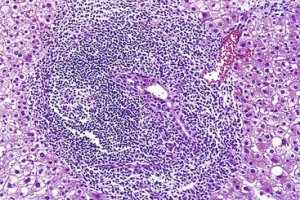 Перспективы применения антигомотоксических препаратов при лечении острых и хронических вирусных гепатитов
Перспективы применения антигомотоксических препаратов при лечении острых и хронических вирусных гепатитов