- Головна
- /
- Статті
- /
- Інфекційні захворювання
- /
- Болезнь Уиппла: клиника, диагностика, лечение
Болезнь Уиппла: клиника, диагностика, лечение
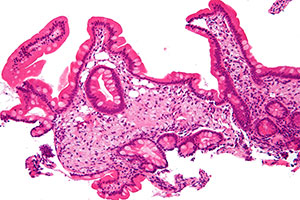
Болезнь Уиппла – редкое мультисистемное заболевание инфекционной природы со множественными клиническими проявлениями. Первым эту болезнь описал американский патологоанатом Джордж Уиппл (George H. Whipple), наблюдавший в аутопсийном материале выраженное увеличение мезентериальных лимфоузлов в сочетании с полисерозитом [14].
При гистологическом исследовании кишечника и лимфоузлов им были выявлены множественные отложения липидов и большое количество макрофагов, содержащих аргирофильные палочкообразные структуры. Автор предположил, что в основе заболевания лежит нарушение метаболизма жира, которое он предложил назвать «интестинальной липодистрофией». В то же время не исключалась и инфекционная этиология болезни. Д. Уиппл указывал на сходство микроорганизмов, найденных в собственной пластинке слизистой оболочки тонкой кишки, с бледной спирохетой. Однако длительное время многие ученые оспаривали инфекционную природу этого заболевания.
Только к середине ХХ столетия постепенно накопились факты, свидетельствовавшие в пользу бактериальной этиологии заболевания. В 1949 г. было установлено, что в биоптатах из лимфоузлов и тонкого кишечника содержатся PAS-позитивные (PAS – periodic acid Schiff) макрофаги с включениями, похожими на продукты распада бактерий [4]. Возбудителями болезни объявлялись многие бактерии, выделявшиеся в культуре из биоптата (коринебактерии, бруцеллоподобные микроорганизмы, L-форма стрептококка и др.). И лишь в 1991 г. R. Wilson с соавт. [15], а затем в 1992 г. D. Realman с соавт. [11] с помощью полимеразной цепной реакции (ПЦР) выделили грамположительную бациллу из материала инфицированных тканей больного, названную Tropheryma whippelii (от греческого trophe – питание, eryma – барьер). По своим филогенетическим свойствам T. whippelii принадлежит к актиномицетам, имеет трехслойную клеточную оболочку, единственную круговую хромосому и небольшой размер генома. Полагают, что патогенными могут быть не все, а строго определенные штаммы возбудителя.
Выявление типичных пенистых макрофагов в периферических лимфатических узлах, печени, легких, ЦНС и других органах, а также вовлечение в патологический процесс сердца и суставов свидетельствует о системном характере заболевания. В патогенезе болезни Уиппла наряду с генерализацией инфекции большое значение придается иммунологическим нарушениям, в частности, изменениям соотношения регуляторных субпопуляций Т-лимфоцитов, утрате способности макрофагов лизировать возбудителя и др.
Болезнь Уиппла – редкое заболевание [1, 2, 3, 13], которым чаще страдают мужчины в возрасте 40-50 лет, однако оно не исключается и в других возрастных категориях. В связи с мультисистемностью заболевания его клинические проявления весьма разнообразны. Блокада лимфатических сосудов тонкой кишки мукополисахаридными комплексами приводит к нарушениям всасывания, вследствие чего развивается диарея (стеаторея), сопровождающаяся приступообразной болью в животе, синдромом мальабсорбции, прогрессирующей потерей массы тела. Частыми проявлениями болезни являются полигиповитаминоз, остеопороз, В12-, фолиево- и железодефицитная анемии, трофические изменения кожи, ногтей, полигландулярная недостаточность [8]. Полиартриты с поражением крупных суставов (коленных, голеностопных, лучезапястных) могут наблюдаться задолго до проявления других симптомов болезни [4].
У большинства больных отмечается мигрирующий олиго- или полиартрит в течение нескольких часов или дней, отличающийся полной ремиссией между приступами. У половины больных в развернутой стадии заболевания наблюдается лихорадка, сопровождающаяся ознобом и профузным потоотделением, а также генерализованная лимфаденопатия. Нередко встречается стойкий кашель, плевриты. В 30-55% случаев поражается сердечно-сосудистая система [12]. Возможно поражение любой из оболочек сердца, но наиболее часто развивается эндокардит. Нередко развивается гипотензия и застойная сердечная недостаточность. Неврологическая симптоматика фиксируется у 10-15% пациентов и может быть как первым проявлением заболевания, так и развиваться спустя годы на фоне манифестной картины болезни Уиппла.
В течении заболевания выделяют 3 стадии:
- I – внекишечные симптомы (лихорадка, полиартрит);
- II – мальабсорбция с прогрессирующим похуданием и тяжелыми метаболическими проявлениями;
- III – системные проявления (неврологическая симптоматика, панкардит, полисерозит).
Полиморфизм клинических проявлений болезни Уиппла обусловливает трудности в постановке диагноза. Нередко диагноз устанавливается спустя несколько лет с момента появления первых симптомов заболевания. Кроме того, затруднена дифференциальная диагностика с другими болезнями тонкой кишки, поскольку клиническая картина болезни Уиппла во многом стереотипна и представлена синдромом мальабсорбции, который сочетает диарею, потерю массы тела, белковую недостаточность и признаки гиповитаминоза. Такие проявления, как анемия, увеличение СОЭ, лейкоцитоз, гипоальбуминемия, нарушения электролитного баланса не являются специфичными признаками одного заболевания.
Диагноз ставится при морфологическом исследовании биоптата слизистой оболочки верхних отделов тонкой кишки. При эндоскопическом исследовании выявляют отек, гиперемию, резкое утолщение складок кишки в связи с лимфостазом, неровность рельефа слизистой из-за желтовато-белых бляшек. При микроскопии биоптатов из двенадцатиперстной и тощей кишок обнаруживают булавовидные ворсинки, содержащие большое количество лимфы, внутри- и внеклеточные скопления жира в слизистой оболочке. Характерно наличие своеобразных ШИК-положительных макрофагов, инфильтрирующих собственную пластинку слизистой оболочки тонкой кишки, и выявление в них бацилл, определяемых при электронной микроскопии [10]. Такие же макрофаги могут обнаруживаться в брыжеечных лимфоузлах, печени, селезенке, сердце, мозговой ткани.
Однако в настоящее время установлено, что выявление PAS-позитивных включений в цитоплазме не является патогномоничным только для болезни Уиппла, а может встречаться у ВИЧ-инфицированных больных, при коринебактериозе, микозах, саркоидозе, гистоплазмозе. В связи с этим особую актуальность приобретает метод ПЦР, позволяющий идентифицировать ДНК T. whippelii как в биоптатах, так и других биологических средах [9, 11]. Определение ДНК возбудителя в кале больных отличается высокой специфичностью (93,3%) и имеет преимущества по сравнению с инвазивными методами [7].
Алгоритм дифференциальной диагностики болезни Уиппла должен включать такие патологические состояния, как лихорадка неясного генеза, различные полиартриты, инфекционный эндокардит, лимфогранулематоз, первичные и приобретенные лимфангиэктазии, глютеновая энтеропатия, болезнь Крона и др. В связи с тем что на ранних стадиях болезнь Уиппла часто скрывается под маской других заболеваний, для правильной постановки диагноза необходимо помнить о тщательном сборе анамнеза, проведении полного физикального обследования больного и использовании современных специфичных методов диагностики. Правильно установленный диагноз является залогом успешного лечения больных.
В настоящее время разработаны схемы базисной антибактериальной терапии болезни Уиппла [13]. По мнению большинства авторов, лечение должно включать бактерицидные антибиотики, хорошо проникающие через гематоэнцефалический барьер. Тетрациклин или его полусинтетический аналог метациклин рекомендуется применять в течение 2-5 месяцев. Затем для поддержания ремиссии следует перейти на интермиттирующую (до 9 месяцев) терапию с приемом препарата через день или 3 дня в неделю с перерывом в 4 дня.
В последние годы в практику лечения болезни Уиппла введен триметоприм-сульфаметоксазол (Бисептол, Ко-тримоксазол). При церебральных поражениях рекомендуется следующая схема терапии: 1,2 млн ЕД бензилпенициллина (пенициллин G) и 1 г стрептомицина парентерально ежедневно в течение 2 недель с последующим назначением Ко-тримоксазола (триметоприм – 160 мг и сульфаметоксазол – 800 мг) дважды в день в течение 1-2 лет до отрицательного результата ПЦР и исчезновения T. whipplii в биоптатах из двенадцатиперстной кишки. Длительная, в течение 1-2 лет, поддерживающая терапия Ко-тримоксазолом считается наиболее успешной в плане профилактики неврологической симптоматики.
В качестве вспомогательной терапии рассматривается назначение кортикостероидов 30-40 мг/сут с последующим постепенным снижением дозы, коррекция метаболических и водно-электролитных расстройств, восполнение дефицита витаминов. Своевременное лечение способствует наступлению ремиссии заболевания.
Литература
- Гребенев А.Л., Мягкова Л.П. Болезни кишечника (современные достижения в диагностике и терапии). – М.: Медицина, 1994. – 400 с.
- Гриценко И.И., Степанов Ю.М., Щербинина М.Б. и др. Клинический разбор случая болезни Уиппла // Сучасна гастроентерологія. – 2003. – № 2 (12). – С. 57-61.
- Логинов А.С., Парфенов А.И., Полев Н.И. Болезнь Уиппла: результаты длительного наблюдения // Тер. арх. – 1998. – Т. 70, № 9. – С. 35-41.
- Ayoub W.T., Davis D.E., Torrery D. et al. Bone destruction and ankylosis in Whipple's disease // J.Rheumatol. – 1982. – № 9. – P. 930-931.
- Black-Schaffer B. The tinctorial demonstration of glycoprotein in Whipple's disease // Proc. Soc. Exp. Biol. Med. – 1949. – № 72. – P. 225-227.
- Dulty F., Altwegg M. Whipple Disease and «Tropheryma whippelii» // Clinical Microbiol. Reviews. – 2001. – Vol. 14, № 3. – P. 561-583.
- Maibach R.C., Dulty F., Altwegg M. Detection of Tropheryma whippelii DNA in feces by PCR using a target capture method // J. of Clinical Microbiology. – 2002. – Vol. 40, № 7. – P. 2466-2471.
- Marth T., Raoult D. Whipple's disease // Lancet. – 2003. – № 361. – P. 239-246.
- Misbuh R., Mapstone N.P. Whipple's disease revisited // J. Clin. Pathol. – 2000. – № 53. – P. 750-755.
- Raoult D., Birg M.C., LaScola B. et al. Cultivation of the bacillus of Whipple disease // N. Engl. J. Med. – 2000. – № 342. – P. 620-625.
- Relman D.A., Schmidt T.M., MacDermott R.P. et al. Identification of the uncultured bacillus of the Whipple disease // N. Engl. J. Med. – 1992. – № 327. – P. 293-301.
- Richardson J.G., Burrows L.L., Korithoski B. et al. Tropheryma whippelii as a cause of afebrile culture-negative endocarditis: the evolving of Whipple's disease // J. Infect. – 2003. – Vol. 47, № 2. – P. 760-766.
- Singer R. Diagnosis and treatment of Whipple's disease (review) // Drugs. – 1998. – № 55. – P. 699-704.
- Whipple G.H. A hitherto undescribed disease characterized anatomically by deposits of fat and fatty acids in the intestinal mesenteric lymphatic tissues // Bull. John Hopk. Hosp. – 1907. – Vol. 18. – P. 382-391.
- Wilson K.H., Blitchington R., Frothingham R. et al. Phylogeny of the Whipple's disease – associated bacterium // Lancet. – 1991. – № 381. – P. 474-475.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення

 Болезнь Крона: причины, симптомы, лечение
Болезнь Крона: причины, симптомы, лечение
 Болезнь Крона
Болезнь Крона
 Внекишечные проявления хронических воспалительных заболеваний кишечника
Внекишечные проявления хронических воспалительных заболеваний кишечника
 Целиакия, болезнь Уиппла – клинические маски
Целиакия, болезнь Уиппла – клинические маски