- Головна
- /
- Статті
- /
- Акушерство, гінекологія, репродуктивна медицина
- /
- Рост и развитие органов человеческого плода: 50 лет исследований
Рост и развитие органов человеческого плода: 50 лет исследований
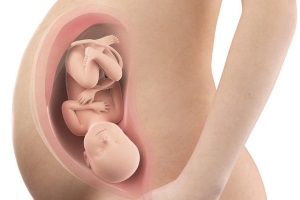
Представления о росте человеческого плода и органогенезе весьма существенно пополнились за последние 50 лет, хотя ряд таких ключевых моментов, как кровоток через сердце и печень плода во внутриутробном периоде и плацентарное кровообращение, были описаны анатомами и физиологами гораздо раньше. Несмотря на это, физиологические исследования на моделях животных были выполнены только в последнем столетии.
Внедрение в научную практику ультразвуковой и допплеровской флуометрии позволило проводить внутриутробные исследования роста и развития человеческого плода, а также оценку кровообращения в его сосудистых бассейнах. Кроме того, в последние два десятилетия изучено снабжение плода кислородом и питательными веществами, что стало возможным благодаря получению проб крови в относительных равновесных состояниях. Эти исследования, наряду с испытаниями, основанными на использовании методики стабильных изотопов, прояснили некоторые аспекты снабжения плода такими важнейшими питательными веществами, как глюкоза, аминокислоты и жирные кислоты. В это же время была установлена роль дисфункции плаценты как основного фактора болезней плода, ведущих к задержке его внутриутробного роста. Позднее доступность таких инструментальных методов визуализации, как трехмерная ультрасонография и электромагнитный резонанс, сделала возможным изучение роста и развития органов плода. Подобные сведения о здоровом плоде расширяют возможности клиницистов в распознании патологических фенотипов различных плодных органов и позволяют корректировать заболевания плода.
В 1950-е годы возможности акушеров относительно наблюдения за внутриутробным развитием плода были весьма скромными, поэтому роды нередко преподносили им сюрпризы в виде рождения близнецов или появления детей с врожденными уродствами.
Тенденция к ретроспективному отслеживанию пути от родов до зачатия, возникшая в те годы, к настоящему времени позволила накопить более глубокие знания о росте и развитии органов плода (относительно структуры и функции), а также его патологии (c учетом ее причин и анамнеза).
Однако столь длинный «акушерский путь» можно было бы пройти гораздо легче и быстрее, если бы специалисты, во-первых, приняли к сведению достижения своих предшественников – анатомов и физиологов (в форме данных сравнительного акушерства); во-вторых – начали рассматривать плод как здоровый субъект, а не фокусировали свое внимание на плодных аномалиях (обобщенно обозначаемых понятием «дистресс-синдром плода»). Вместо этого акушеры в первую очередь ринулись изучать болезни плода; подобный неверный подход и привел к появлению формулировок наподобие «плод как пациент» и др.
Как известно, базисом медицины является определение понятия «здоровье», сегодня это также должно стать основной целью акушерства.
Уроки анатомии
Большинство сведений об органах плода накоплены в течение многих лет и давно известны анатомам [1]. Еще Аранцио и Гарвей (соответственно в XVI и XVII ст.) знали, что маточные (материнские) и пупочные (плодные) кровеносные сосуды не состыковываются непосредственно друг с другом в пределах плаценты. Однако именно Гарвей установил факт циркуляции крови, а также то, что движение крови у плода осуществляется по двум каналам – через овальное отверстие и артериальный проток, что позволяет двум желудочкам сердца работать параллельно, перекачивая кровь из крупных вен в артерии. В то же время стало очевидным, что некоторое количество артериальной крови циркулирует в тканях плода, а остальная часть – в плаценте.
В XVIII веке Вольф предположил, что почти две трети объема кровотока через нижнюю полую вену может поступать в левое предсердие через овальное отверстие, а остальной объем поступает в правое предсердие. Он не считал, что евстахиев клапан является ключевым фактором кровообращения плода, и отчетливо продемонстрировал смешивание двух потоков крови из полых вен внутри правого предсердия, хотя только кровь из нижней полой вены поступает в левое предсердие [1].
В 1564 году, еще до появления гипотезы гемодинамики плода, предложенной Вольфом, Везалий опубликовал первое описание венозного протока, которое ошибочно приписывают Аранцио. Венозный проток берет начало из ствола, образованного пупочной и воротной венами, и направляется, практически окруженный паренхимой печени, к соединению главных печеночных вен с нижней полой веной [1]. Везалий определил, что по ширине он составляет менее половины сечения пупочной вены, и продемонстрировал отток из венозного протока непосредственно в правое предсердие [1].
В 1753 году Бертин использовал инъекции расплавленного воска для изучения отношения венозного протока к печеночным сосудам. Тем не менее, только 50 лет спустя было выполнено несколько прямых наблюдений на живых плодах млекопитающих (внутриутробно или после родов) – Рудольф и соавт. [2] описали сосудистую сеть печени плода и кровообращение у плодов овец, используя инъекции силиконового каучука. Печеночный кровоток у плода на этой модели осуществляется через пупочную вену, а также через воротную вену и печеночную артерию. Пупочная вена входит в ворота печени и дает воротные ветви к левой доле печени. Венозный проток образуется в месте, где пупочная вена изгибается вправо, соединяясь с воротной веной и образуя затем воротные ветви к правой доле печени. Левая печеночная вена присоединяется к венозному протоку непосредственно перед соединением с нижней полой веной, тогда как правая печеночная вена соединяется с нижней полой веной отдельно.
Опыты, выполненные Рудольфом и соавт. на моделях животных [2], указали путь для дальнейших исследований с использованием методики допплерографии, которая позволила изучить и описать кровообращение и распределение кровотока в различных органах человеческого плода. Эти исследования очень ярко проиллюстрировали основные особенности кровообращения у плода.
Уроки физиологии
Чтобы рассматривать плод как здоровый субъект, следует начать с изучения специфической физиологии его органов. В 1940-х годах Баркрофт вычислил базисный уровень потребления кислорода для многих тканей плодов овцы различных гестационных возрастов, продемонстрировав, что значения этого показателя повышаются для мозговой ткани с 3,4 на 99-й день до 8,3 на 144-й день (в мл/мг сухого веса в час), снижаются для мышечной ткани (с 3,1 до 0,7 мл/мг сухого веса в час) и остаются практически неизменными для печеночной ткани (порядка 7,3 мл/мг сухого веса в час) [3]. Позднее Батталья и Месчия определили маточную и пупочную утилизацию кислорода у беременных овец с постоянными катетерами, получив значения 2,16 ммоль/мин для маточного потребления кислорода и 1,18 ммоль/мин для пупочного, вычислив таким образом величину утероплацентарного потребления O2, которая составила 0,98 ммоль/мин [4]. Эти наблюдения, проведенные in vivo, подчеркивают очень высокий уровень метаболизма в плаценте, которая поглощает почти такое же количество кислорода, как и плод.
С недавних пор совершенствование методики УЗИ сделало возможным внутриутробное измерение пупочного кровотока у плода человека. Объемная скорость кровотока в пупочной вене вычисляется по площади сечения пупочной вены и линейной скорости пупочного кровотока (рис. 1). Значения пупочного кровотока, измеренного этим методом во второй половине физиологической беременности, колебались в диапазоне от 70 до 100 мл/кг/мин к моменту родов [5-9]. Затем оценивали пупочное потребление кислорода как производную пупочного кровотока и пупочную венозно-артериальную разницу по кислороду. При беременности в нормальные сроки потребление кислорода плодом человека находится в пределах 0,25-0,35 ммоль/мин/кг (или 0,9-1,2 ммоль/мин), что сопоставимо со значениями, полученными в эксперименте на овцах.
С учетом роли плаценты важным показателем представляется градиент кровяного давления в пупочной артерии и вене, который является движущей силой кровотока в плацентарных сосудах. До настоящего времени прямое измерение артериального давления (АД) возможно только в эксперименте у плодов животных; проводить же аналогичное измерение в сосудах пуповины или в сосудистых бассейнах плода человека не представляется возможным. Тем не менее, даже относительно методики измерения этих параметров на моделях животных были отмечены некоторые несоответствия. Впрочем, с учетом надлежащих корректив Баркрофту [3] удалось установить, что в период беременности АД у плода повышается, тогда как его венозное давление остается достаточно стабильным, создавая таким образом гидродинамический градиент, среднее значение которого повышается с 15 мм рт. ст. на 60-й день беременности до 40 мм рт. ст. к моменту рождения.
Изменения маточно-плацентарной перфузии в период беременности у человека в течение последних двух десятилетий исследовали непрямым методом, определяя профили кровотока посредством допплеровской флоуметрии [10-12]. Благодаря этому методу было установлено уменьшение кровотока как в маточных, так и в пупочной артериях при внутриутробной задержке роста плода (IUGR). Эти исследования, особенно касающиеся пуповинного кровообращения, стали значительным вкладом в современные достижения по контролю за беременностью высокого риска [10]. При нормальной беременности ветви маточных артерий трансформируются в маточно-плацентарные сосуды, обладающие малым гидродинамическим сопротивлением (низкорезистентные сосуды). Нарушения этого процесса отмечались в биоптатах плаценты при беременности, протекавшей с IUGR; они ассоциировались с признаками двухсторонней высокорезистентной формы волны скорости потока с ранними диастолическими инцизурами на 24-й неделе беременности [10, 11]. Патологическая форма волны при допплеровском исследовании пупочной артерии предположительно отражает аномальное плацентарное сопротивление, вызванное изменениями морфологии сосудов ворсинок, и отчетливо коррелирует с повышением перинатальной смертности [10].
Не так давно были проведены измерения АД совместно с допплеровской флоуметрией пупочной артерии у беременных овец с установленными постоянными катетерами и индуцированной IUGR по модели тепловой камеры, разработанной в Денвере [13]. По сравнению с контрольной беременностью, беременность с IUGR характеризовалась повышенным системным АД, сниженным пупочным кровотоком, повышенными индексами допплеровской флоуметрии для пупочной артерии и аорты, а также сниженным плацентарным сосудистым сопротивлением.
Интересно, что допплеровский индекс сопротивления пупочной артерии (систоло/диастолическое соотношение) отчетливо коррелирует с величиной системного АД (рис. 2). В этих исследованиях на животных in vіvo выявлено, что для плодов с IUGR характерна гипертензия и что повышенные допплеровские индексы сопротивления пупочной артерии соответствуют фетоплацентарному гипертензивному состоянию. Весьма вероятно, что последующие стадии заболевания, в которых страдает кардиогемодинамика, сопровождаются снижением АД. Изменения кровяного давления могут привести к необратимым изменениям в клеточной линии пуповины и сосудов плода и послужить причиной повышенного риска сердечно-сосудистой патологии во взрослой жизни; они отчетливо коррелируют со степенью развития плода перед родами [14, 15]. Недавно выявлены генетические изменения в эндотелиальных клетках пупочной вены, задействованных в регуляции кровотока, в условиях гипоксии [16] и сахарного диабета [17].
Возникновение сосудистых рефлексов также стало объектом научных исследований, ориентированных на изучение физиологии плода. В экспериментальном определении изменений уровня АД у плодов коз выявлено, что непосредственно в момент перевязывания пуповины или в ближайшее время после этой манипуляции частота сердечных сокращений плода замедляется [3]. Известно, что в клиническом акушерстве подобная процедура является общепринятой практикой.
Существует мнение о том, что данное явление – следствие асфиксии, ведущей к блокаде сердца. Баркрофт [3] с помощью ваготомии доказал, что первая фаза брадикардии при вариабельном замедлении сердечного ритма после пережатия пуповины обусловлена активацией блуждающего нерва. Дальнейшие сведения о реакции плода на изменения, происходящие при замедлении ритма сердечных сокращений, были получены благодаря изучению времени внутрисердечного проведения при электрофизиологических исследованиях. Сообщалось об изменении характера зубца P и продолжительности интервала PQ на ЭКГ во время вариабельного замедления ритма, когда частота сердечных сокращений плода снижается до 80-60 сокращений в минуту на протяжении 10-20 с и более. В начале замедления интервал РQ постепенно укорачивается, тогда как зубец Р становится двухфазным или полностью исчезает [18]. Подобные явления свидетельствуют о включении вагусного механизма, который ведет к угнетению активности синоатриального узла с миграцией функции водителя ритма от него к атриовентрикулярному узлу.
Вероятно, начинать рассмотрение органов плода целесообразно с оценки взаимосвязанных с ними объема кровотока плаценты и фетоплацентарного метаболизма.
Объем плаценты
Рост и развитие плаценты и питаемого ею здорового плода имеют значительные отличия.
У овец, как описано Баркрофтом, в зависимости от внутриутробного (гестационного) возраста масса плода увеличивается в основном во второй половине беременности, поскольку котиледоны растут быстрее в первой ее половине, а затем остаются практически неизменными до конца беременности [3].
Доказательства того, что плацента достигает своих максимальных размеров задолго до конца беременности, были получены и в результате изучения других видов животных, в частности коз и кроликов.
У человека же различия между скоростью роста плода и плаценты в период беременности характеризуются большим увеличением соотношения массы плода/плаценты [19]. Однако, в отличие от овец, у которых максимальная масса плаценты достигается к середине беременности, у человека развитие плаценты происходит по S-образному регрессивному графику, а рост плода при этом описывается экспоненциальной кривой с максимальной точкой в период третьего триместра [19]. Рост плаценты сопровождается множеством изменений, связанных с созреванием, включая значительное увеличение общей площади поверхности плаценты и уменьшение ее толщины [20], что в совокупности ведет к увеличению плацентарной проницаемости для питательных веществ. К тому же в период беременности происходят значительные изменения активности множества плацентарных транспортных систем, в особенности микроворсинчатой мембраны, что отмечается после первого триместра беременности [21, 22].
С недавних пор появилась возможность оценивать объем и рост плаценты в период беременности методом трехмерной ультрасонографии (рис. 3). Объем плаценты увеличивается со средней величины около 16 мм на 10-й неделе до 200 мм на 23-й неделе беременности. Следовательно, соотношение между массой плода и плаценты на 23-й неделе приблизительно равно 2, а к концу нормальной беременности – около 6. Любопытен тот факт, что у 17 плодов с хромосомной аномалией (трисомия 21 пары) отмечено уменьшение объема плаценты по сравнению с нормальными плодами аналогичного гестационного возраста (рис. 4). В исследованиях, проведенных во время родов, установлено, что для недоношенных новорожденных объем плаценты и соотношение масса тела/плаценты были меньше, чем у детей с той же массой тела, родившихся в срок [19]. Предварительные данные свидетельствуют о том, что если при нормальной беременности сниженная масса плаценты не ассоциируется со значительным уменьшением массы тела плода, то при беременности, протекающей с IUGR, существует отчетливо выраженная связь между сниженной массой плаценты и дефицитом массы плода, особенно в наиболее тяжелых случаях IUGR. С другой стороны, снижение массы плаценты и значения плодно/плацентарного весового соотношения описано при беременности, осложненной гестационным сахарным диабетом [23], причем даже при обеспечении оптимального уровня гликемии у матери на протяжении всего третьего триместра [24]. Следовательно, есть основания полагать, что объем плаценты, измеренный во втором триместре беременности, будет достоверно коррелировать с массой новорожденного [25, 26].
Кровообращение
Степень взаимоотношения между маточной и пупочно-плацентарной перфузией имеет решающее значение для эффективного обмена веществ и определяется так называемой равномерной или неравномерной плацентарной перфузией. В идеальной ситуации система равномерной перфузии представлена пропорциональными потоками маточного и пупочного кровоснабжения. Неравномерное кровоснабжение характеризуется перфузией плацентарного котиледона, непропорциональной с маточной и пупочной стороны, что определяет неэффективность обмена веществ.
До сих пор нет инструментальных методов, позволяющих оценить это функциональное состояние в период беременности, также неизвестно, что происходит in vivo в патологических ситуациях, подобных инфаркту плаценты. Другой интересный аспект маточной и пупочной перфузии – представляют ли они противоточную или сходящуюся систему? Пространственная конфигурация маточных и пупочных сосудов была описана для котиледона овечьей плаценты. Максимальная эффективность достигается, вероятно, двумя капиллярными потоками, текущими в противоположных направлениях при уравновешенных значениях пупочного и маточного артериального кровотока. Тем не менее, эти данные нельзя экстраполировать на беременность у человека. Одновременно измерены газовый состав артериальной и венозной крови из маточных и пупочных сосудов в момент проведения элективного кесарева сечения в конце беременности [27]. Как показано на рисунке 5, значение pО2 для крови из пупочной вены положительно коррелировало с pO2 маточной венозной крови и всегда было ниже последнего, что дает основания полагать о преобладании в плаценте человека сходящейся системы с двумя уравновешенными путями плацентарного венозного оттока. Кроме того, беременность с IUGR характеризовалась достоверно повышенным градиентом давления между маточными и пупочной венами по сравнению с нормальной беременностью. Поскольку коэффициент потребления кислорода маткой был достоверно снижен, а в оттекающей от беременной матки венозной крови сохранялся высокий уровень кислорода, эти данные в совокупности свидетельствуют о том, что снижение уровней кислорода, наблюдавшееся у плодов при IUGR, отражает нарушение не плацентарной перфузии, а проницаемости плаценты. Тем не менее, гипоксия не является постоянной характеристикой IUGR. В соответствии с классификацией IUGR, основанной на допплеровской флоуметрии пупочной артерии и определении частоты сердечных сокращений плода, установлено, что гипоксия и гиперлактацидемия отмечаются у одной трети плодов с повышенным пульсационным индексом пупочной артерии и у двух третей плодов с нарушениями пупочного кровотока в сочетании с изменениями частоты сердечных сокращений [28].
Фетоплацентарный метаболизм
На протяжении всего внутриутробного периода плацента является органом, обеспечивающим сопряжение плода с материнским организмом, играющим ключевую роль в процессе питания плода до момента рождения. Следовательно, плацента – это плодный орган, хотя с точки зрения питания плода беременность можно рассматривать как трехкомпонентную модель, включающую мать, плаценту и плод, каждый из которых имеет свой собственный метаболизм, но в то же время взаимодействует со всеми остальными [29].
Питание плода зависит от его снабжения питательными веществами, поступающими из организма матери через пупочно-плацентарное кровообращение. Рост и развитие плода регулируется за счет баланса между потребностью плода в питательных веществах, определяемой его генетическим потенциалом роста, и степенью обеспечения за счет плаценты и организма матери. К факторам, определяющим уровень материнско-плацентарного снабжения плода питательными веществами, относятся характер питания и метаболизм организма матери, градиент концентраций в организмах плода и матери, маточно-плацентарный кровоток, размер плаценты и ее транспортные возможности [29].
Глюкоза, аминокислоты и жирные кислоты являются важнейшими питательными веществами в жизнедеятельности плода, необходимыми как для депонирования в тканях, так и в качестве энергетического субстрата для окислительных процессов. Невозможно рассматривать плацентарный метаболизм в отрыве от метаболизма плода и матери, поскольку плацента находится в центре множества метаболических процессов. Тем не менее, следует иметь в виду, что плацентарные клетки (трофобласты) являются плодными клетками. Этот факт свидетельствует о том, что плацента – составная часть плодной системы, обеспечивающей обратную связь с плодом.
Многое из того, что известно о снабжении питательными веществами плода человека, было описано в течение последних 20 лет на основании данных, полученных при заборе проб плодной крови. Содержание кислорода в крови пупочной вены остается неизменным на протяжении второй половины беременности [30]. Это является результатом синхронного повышения концентрации гемоглобина и снижения pО2 в венозной крови пуповины.
Облегченная система диффузии, отвечающая за поступление глюкозы от матери к плоду, опосредуется белками семейства глюкозных транспортеров (GLUT), локализованных как на материнской, так и на плодной поверхности мембран [31]. При нормальной беременности концентрация глюкозы в крови плода прямо зависит от концентрации ее в крови матери и от гестационного возраста [32], при этом плацента потребляет значительное количество глюкозы [33]. У плодов при IUGR не отмечается снижения средней концентрации глюкозы по сравнению с нормальными плодами. Кроме того, забор образцов крови плода при IUGR не выявил значимого глюкогенеза в плодном сегменте при проведении матери постоянной инфузии UL-13C-глюкозы [34]. Однако градиент концентраций глюкозы в крови матери и плода был значительно повышен у плодов с нарушениями пупочного артериального кровотока и частоты сердечных сокращений [32]. С другой стороны, результаты предварительных наблюдений in vivo подтверждают, что концентрация глюкозы в венозной крови пуповины достоверно повышается даже при эффективно компенсированном гестационном сахарном диабете у матери, когда уровень глюкозы в материнской крови сопоставим с уровнем того же субстрата в крови у здоровых беременных [35]. Это может либо указывать на вклад возрастающего трансплацентарного транспорта глюкозы, либо свидетельствовать об изменении фетоплацентарного метаболизма глюкозы у беременных с гестационным сахарным диабетом.
Транспорт жирных кислот от матери к плоду представляет собой значительно более сложный комплекс. Хотя сочетание жирных кислот, доставляемых плоду, в основном определяется профилем жирных кислот в материнской крови, плацента способна избирательно передавать плоду арахидоновую и докозагексаеновую кислоту, что обеспечивается комбинированным действием различных механизмов [36, 37]. Несмотря на то что все жирные кислоты способны проникать через липидный бислой посредством простой диффузии, идентифицировано множество транспортных протеинов, связывающих жирные кислоты (FABPs) [38]. Незаменимые жирные кислоты поступают в плаценту главным образом в виде неэстерифицированных жирных кислот, транспортируемых триглицеридами из липопротеинов материнской жировой ткани и печени [39]. Они высвобождаются под действием липопротеинлипазы (ЛПЛ), активность которой выявлена и в плаценте человека [40].
Установлено, что уровень экспрессии ЛПЛ матричной РНК (мРНК) при IUGR достоверно повышен, особенно в тех случаях IUGR, которые сопровождаются нарушением пупочного артериального кровотока [41]. В отличие от полученных результатов, Магнуссон и соавт. [42] ранее сообщали о снижении активности ЛПЛ в плацентарных микроворсинчатых мембранах при IUGR. Таким образом, увеличение экспрессии ЛПЛ мРНК можно рассматривать как компенсаторный механизм. Изменения экспрессии ЛПЛ могут быть связаны с изменениями обмена жирных кислот в плаценте и способствовать патологическим взаимоотношениям полиненасыщенных жирных кислот у плода и матери, что описано при заборе образцов плодной крови в случаях беременности, протекающей с IUGR [43].
Плацента также имеет специфические места для связывания липопротеинов различной плотности (очень низкой, низкой, высокой), переносящих эстерифицированные липиды. Сообщалось об изменениях рецепторов, задействованных в плацентарном захвате холестерина при тяжелых формах IUGR, что ассоциировалось с изменениями уровней холестерина и липопротеинов низкой плотности (ЛПНП) в крови матери [44].
Многими исследователями очерчен диапазон отчетливых изменений плаценты, выявленных при беременности, ассоциированной с IUGR, которые также становятся вероятными при наличии избыточного роста плода.
Особенно полно эти изменения (как in vivo, так и in vitro) описаны для метаболизма аминокислот; они включают снижение концентрации аминокислот и активности их плацентарных транспортных систем при беременности, протекающей с IUGR [45-47], а также повышение их концентрации и транспорта при сахарном диабете [48, 49].
Аминокислоты проникают через плаценту благодаря комплексному механизму, включающему функционирование переносчиков, расположенных на ворсинчатой и базальной мембранах, плацентарный матаболизм, а также неосинтез заменимых аминокислот в плаценте. В результате комплексного действия указанных механизмов осуществляется активный транспорт аминокислот, который обеспечивает их более высокие концентрации в крови плода по сравнению с концентрацией в крови матери на протяжении второй половины беременности [50, 51].
При беременности с IUGR наблюдалось достоверное снижение концентрации аминокислот, особенно незаменимых аминокислот с разветвленной цепью, независимо от степени тяжести состояния [28, 52], с достоверным снижением плодно/материнского соотношения.
Кинетика этих механизмов изучена in vivo в равновесном состоянии с помощью проведения матери постоянной инфузии 1-13C лeйцина перед забором проб крови у плода [53]. На рисунке 6 представлены результаты, полученные для нормальной беременности и беременности с IUGR, разделенных по степени тяжести. При нормальной беременности, поскольку лейцин является незаменимой аминокислотой, разведение метки (приблизительно на 20%) в кровотоке плода объясняется катаболизмом белка, тогда как при беременности с IUGR этот показатель прогрессивно и достоверно повышался, указывая на то, что помимо уменьшения плацентарного транспорта при IUGR также пропорционально увеличивается катаболизм белка; это можно рассматривать как признак декомпенсации плода.
Эти данные свидетельствуют о том, что изменения со стороны плаценты человека могут быть распределены в группы или фенотипы, ассоциирующиеся со специфическими особенностями роста плода [47]. Идентификация плацентарных фенотипов, соответствующих различным типам роста плода, позволит полнее раскрыть процесс его роста и поможет клиницистам в выявлении беременности с риском аномалий плодного роста.
Сердце и кровообращение
Дэйвс 50 лет назад рассчитал, что сердечный выброс у плодов овец составляет 315 мл/кг/мин. Из них 142 мл/кг/мин (45%) приходится на правый, а 174 мл/кг/мин (55%) – на левый желудочек сердца [54]. Измерение максимальной скорости кровотока в сердечных сосудах у плодов человека позволило вычислить значение объемной скорости кровотока, которая в легочной артерии составила 600 мл/мин, в аорте – 450 мл/мин. Сумма двух этих показателей составляет приблизительно 1050 мл/мин, или около 300 мл/мин/кг, что вполне сопоставимо со значениями, полученными Дэйвсом для плодов овец.
Кроме сердечного выброса, сегодня можно оценить распределение крови по разным органам плода человека, в частности пупочный, мозговой, печеночный и внутрисердечный кровоток. Использование допплеровского метода позволило описать временную последовательность патологиченских изменений плодного кровообращения в подгруппах плодов с начальной и тяжелой задержкой внутриутробного роста [55]. В этом исследовании тяжелая задержка внутриутробного роста у плодов сопровождалась прогрессирующей последовательностью выявления отклонений, которые относили к категории «ранних» и «поздних». Ранние изменения происходили в периферических сосудах (пупочных и средних мозговых артериях; в 50% случаев поражение развивалось за 15-16 дней до родов). Поздние изменения включали обратный кровоток в пупочной артерии и патологические изменения венозного протока, аортального и пульмонального путей оттока (в 50% случаев поражения развивались за 4-5 дней до родов). Подобные прогрессирующие изменения отражают тот факт, что заболевания плода, сопровождающиеся задержкой его внутриутробного роста, начинаются как адаптация плода, но затем переходят в расстройство. Поздние изменения достоверно ассоциируются с перинатальной смертью и поэтому требуют экстренного родоразрешения.
Органы плода
Большинство знаний о внутриутробном развитиии, накопленных сегодня, относится к плаценте, сердцу и кровообращению плода. Главным образом, это является результатом доступности тканей (плацента) и методов (исследование частоты сердечных сокращений и допплеровская флоуметрия).
Тем не менее, инструментальные методы исследования открывают новые перспективы в изучении развития и функционирования органов плода. Обратим внимание на доступные данные о двух наиболее важных органах плода – мозге и печени.
Мозг
Важность роста и развития головного мозга плода подтверждается простым наблюдением: у всех видов животных, и особенно у человека, отношение массы мозга к массе тела значительно выше у новорожденных, чем у взрослых особей [56].
При оценке роста мозга методом трехмерной ультрасонографии было установлено, что медиана массы головного мозга составляет приблизительно 15% от общей массы плода. Сонографическое измерение объема головного мозга плода продемонстрировало примерно десятикратное его увеличение на протяжении второй половины беременности [5#]. При заболеваниях плода, в том числе при IUGR, рост мозга сохраняется даже при снижении пупочного кровотока, при этом замедление темпов увеличения объема мозга пропорционально гораздо менее выражено, чем других органов (например, печени) [8].
Магнитно-резонансная визуализация (MRI) является высокоэффективным методом оценки развития и функционирования мозга. В особенности это относится к определению измеряемого коэффициента диффузии воды в человеческом мозге методом диффузионно-весовой магнитно-резонансной визуализации, позволяющем получить ценную информацию о нормальном развитии головного мозга, в частности о размере и направлении немиелинизированных и миелинизированных путей в головном мозге плода во второй половине беременности [58]. Полосы мигрирующей глии, которые могут быть визуализированы, являются весьма важными маркерами нормального развития головного мозга, особенно его белого вещества [59]. Равномерное появление полос около желудочков головного мозга и их взаимосвязь с созреванием плода соответствуют результатам гистологических исследований (рис. 7) [60]. Результаты данных исследований с использованием магнитно-резонансной визуализации демонстрируют наличие мигрирующих глиальных клеток в белом веществе, окружающем желудочки головного мозга у плодов с гестационным возрастом свыше 20 недель, когда миграция нейронов в кору головного мозга уже завершена. Более того, тогда как пренатальное ультразвуковое исследование имеет низкую чувствительность в выявлении гипоксически-ишемических нарушений, метод диффузионно-весовой магнитнорезонансной визуализации позволяет проводить внутриутробную диагностику острых ишемических повреждений головного мозга плода [61].
Тем не менее, анализ частоты сердечных сокращений плода и сегодня продолжает оставаться наиболее доступным методом оценки его неврологического статуса. В действительности вариабельность частоты сердечных сокращений плода следует рассматривать как индикатор функционального сотояния не столько сердечно-сосудистой, сколько нервной системы. Среднее значение вариабельности частоты сердечных сокращений менее 1 удара в минуту четко указывает на утрату регулирующего влияния вегетативной нервной системы на частоту сердечных сокращений и должно рассматриваться как признак центральных неврологических повреждений [62].
Печень плода
Как это уже упоминалось в разделе «Сердце и кровообращение», печень плода расположена в очень специфическом циркуляторном пересечении. Кроме того, она участвует во множестве метаболических процессов, а также в метаболических и эндокринных циклах с плацентой. Следовательно, оценка развития и функционального состояния печени важна для понимания физиологии плода и оценки его благополучия.
На рис. 8 приведены результаты недавно проведенного внутриутробного определения объема печени плода методом трехмерной ультрасонографии. По результатам, полученным с помощью данного метода, увеличение объема печени у здоровых плодов с 18 недели беременности до момента родов описывается экспоненциальным графиком [7]. В то же время получено подтверждение того, что патология плода, ведущая к нарушению его роста, ассоциируется с пропорционалными изменениями объема его печени, уменьшение и увеличение которого было отмечено при IUGR и инсулинзависимом сахарном диабете соответственно [8].
Кровоток в правой доле печени увеличивался с 20 до 45%, тогда как в левой оставался примерно постоянным (40%). Эти изменения обусловлены различными моделями увеличения диаметров пупочной вены и венозного протока в процессе роста и подтверждают гипотезу о том, что венозный проток играет менее важную роль в шунтировании хорошо насыщенной кислородом крови в мозг и миокард в конце нормальной беременности, чем на ее ранних сроках, что ведет к повышенной перфузии печени плода. Однако при задержке роста после начального периода адаптации шунтирование через венозный проток повышено, представляя промежуточный этап перед повреждением [9]. При более тяжелой IUGR процент пупочного кровотока, шунтируемого через венозный проток, больее чем 90 процентиль у контрольных плодов. Это сочетается с одновременным снижением процента кровотока в правой доле печени, с обратным кровотоком из правой доли и воротной системы в венозный проток, что подтверждается как расчетными значениями объема кровотока, так и прямым определением формы пульсовой допплеровской волны [9].
Таким образом, эти изменения обеспечивают относительно постоянное кровоснабжение сердца и головного мозга за счет перфузии печении плода.
Подтверждением этих данных является то, что отношение объемов головного мозга/печени в норме существенно уменьшается с гестационным возрастом и достоверно выше у плодов с задержкой роста, с достоверным обратно пропорциональным отношением между весозависимым объемом пупочного венозного кровотока и соотношением объемов головного мозга/печени у плода [7].
Выводы
За прошедшие 50 лет мы узнали человеческий плод как здоровое существо с большим мозгом. В дальнейшем очень важно восполнить познания и составить завершенную картину морфологического и функционального развития отдельных органов плода. Плацента – плодный орган, играющий ключевую роль в регулировании роста и развитии плода. Следовательно, патология плода намного раньше проявляется в плаценте и лишь затем развивается собственно у плода.
 Какие исследования нужны во время беременности и зачем?
Какие исследования нужны во время беременности и зачем?
 Изменим жизнь людей с диабетом к лучшему
Изменим жизнь людей с диабетом к лучшемуIV Международный медицинский конгресс «Диабет и беременность». 29-31 марта, Стамбул
 Гормональные аспекты невынашивания беременности
(По материалам Международной конференции «Невынашивание беременности – новое понимание старых проблем»)
Гормональные аспекты невынашивания беременности
(По материалам Международной конференции «Невынашивание беременности – новое понимание старых проблем»)
 Проблема выкидыша и замершей беременности или по ком звонит колокол?
Проблема выкидыша и замершей беременности или по ком звонит колокол?
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення
