- Головна
- /
- Статті
- /
- Ендокринологія. Цукровий діабет
- /
- Пухлини коркового шару наднирків
Пухлини коркового шару наднирків
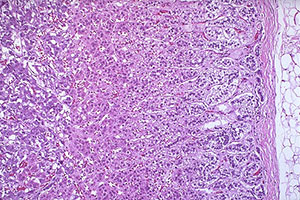
Пухлини кори надниркових залоз відносять до числа найбільш тяжких і складних форм ендокринної хірургічної патології. Вони характеризуються поліморфною клінічною симптоматикою, зумовленою ефектом гормонів та продуктів пухлинного метаболізму.
МКХ-10: D35.0, С74.0, E26.0
Общая информация
Уточнених даних стосовно частоти пухлин наднирників не виявлено, оскільки не завжди вчасно ця патологія діагностується або ж діагностується випадково. У структурі хірургічної патології наднирникових залоз на частку пухлин кори припадає 35-40%. Частота пухлин наднирників при аутопсії коливається від 1,4 до 9%, а за даними КТ становить від 0,4 до 4,4%. Спостерігається зростання частоти захворюваності серед дітей до 5 років та у хворих старших за 40-50 років. Пухлини наднирників частіше бувають у жінок (58,6%), ніж у чоловіків (41,4%). За епідеміологічними дослідженнями, ризик виникнення пухлин наднирників збільшується в чоловіків, якщо вони палять, та у жінок у разі використання ними оральних контрацептивів.
Етіологія, патогенез, чинники ризику
Пухлини наднирників часто діагностуються випадково під час проведення обстеження з приводу інших захворювань (хронічний гепатит і панкреатит, нирковокам’яна хвороба тощо). Приблизно в 1% людей у загальній популяції виявляють пухлини наднирника діаметром від декількох міліметрів до 20 см і більше, при цьому без специфічних клінічних проявів. Такі пухлини називають «інциденталомами» наднирників. Доброякісні та злоякісні пухлини наднирників можуть бути як гормонально неактивними, так і проявляти гормональну активність – виробляти кортизол, альдостерон, андрогени, естрогени.
Етіологія пухлинного росту не встановлена, хоча є дані про хромосомні порушення (генні мутації та делеції), активацію онкогенів, чинніків росту пухлин, що можна вважати вірогідним механізмом молекулярного патогенезу.
У випадку гормонально активних пухлин патогенез захворювання залежить від виду гормонів, які секретує пухлина. Більшість гормонально активних пухлин секретують кортизол, рідше – андрогени, естрогени чи альдостерон. Змішані форми гормональної секреції зустрічаються майже в 75% випадків. Залежно від превалюючої гормональної секреції виділяють 4 основні синдроми гіперкортицизму:
- Синдром Іценка-Кушинга – гіперпродукція глюкокортикоїдів.
- Синдром вірилізації (адреногенітальний синдром) – гіперпродукція андрогенів.
- Синдром фемінізації – гіперпродукція естрогенів.
- Гіперальдостеронізм – гіперпродукція мінералокортикоїдів.
Найчастіше зустрічається комбінація синдрому Іценка-Кушинга з вірильним синдромом.
Клиническая картина
Серед усіх гормонально активних пухлин кори наднирників найпоширенішою є кортикостерома, яка в значній кількості синтезує глюкокортикоїди (переважно кортизол) і мінералокортикоїди, а також андрогени і частково естрогени.
Кортикостерома (глюкостерома). Клінічна картина патології зумовлена порушенням функції системи гіпоталамус-гіпофіз-надниркові залози з вираженими ознаками гіперкортицизму, який ідентичний із синдромом Іценка-Кушинга, основні синдроми якого представлені на схемі 1.
Перебіг злоякісної гормонально активної пухлини наднирника характеризується швидким наростанням симптоматики і прогресуючим погіршенням стану хворих, що помітно відрізняє цю патологію від аналогічних за клінікою захворювань на ґрунті доброякісних аденом наднирників (адренокортикальні аденоми) і гіперпластичних процесів у надниркових залозах (хвороба Іценка-Кушинга).
Слід зазначити визначену послідовність розвитку клінічних синдромів при гормонально активних пухлинах наднирників. Ранніми ознаками пухлин з клінікою синдрому Іценка-Кушинга є порушення статевої функції, так званий гетеросексуальний синдром (від 77 до 100%): розлади менструального циклу (аж до стійкої аменореї і безплідності), зниження лібідо у жінок і потенції у чоловіків, різного ступеня гірсутизм й облисіння волосяної частини голови, наявність висипання на шкірі (acnae vulgaris) як у жінок, так і у чоловіків, можлива лакторея (до 23% випадків).
У хворих спостерігається виражене диспластичне ожиріння з переважним скупченням жиру в ділянці обличчя, плечового поясу, передньої черевної стінки, зі схудненням кінцівок за рахунок проксимальних аміотрофій; гіперемія й одутлість обличчя (матронізм). Шкіра стає сухою, тургор її знижується, з’являються типові широкі, звиті, синюшно-багряні смуги розтягання («стриї»), що локалізуються на тулубі, кінцівках. Часто відмічають трофічні процеси на шкірі гомілок.
Синдром артеріальної гіпертензії інколи супроводжується розвитком недостатності кровообігу, серцево-судинними порушеннями.
До розладу статевої функції, збільшення маси тіла, гіпертонії, зміни шкірного покриву і зовнішності згодом додаються остеопороз, розлад вуглеводного обміну (від порушень толерантності до вуглеводів до стероїдного ЦД). Клінічна картина доповнюється вираженим астено-депресивним синдромом, різкою слабкістю, болями в попереку, кінцівках, головним болем.
Андростерома. Ці пухлини в значній кількості секретують андрогени – дегідроепіандростерон (ДЕА) і дегідроепіандростерон-сульфат (ДЕА-с), які є маркерами андрогенів надниркових залоз, а також андростендіон, 11-ОН-андростендіон, тестостерон, що і зумовлює клінічну картину. У жінок пухлини діагностуються вдвічі частіше, ніж у чоловіків. Часто ці пухлини злоякісні, тож навіть після видалення можуть рецидивувати. Бувають випадки проростання капсули злоякісної пухлини та її розповсюдження на тканину нирки. Метастазує злоякісна андростерома в легені, печінку, нирки.
Першими клінічними ознаками андрогенпродукуючої пухлини наднирників є порушення статевої функції, а потім додаються явища маскулінізації й дефемінізації. Найчіткіше вірильний синдром виявляється у жінок у вигляді гіпоплазії молочних залоз, зміни тембру голосу, появи акне на шкірі, випадіння волосся на голові, гіпертрофії клітора. Паралельно відзначається аменорея, безплідність, часто – артеріальна гіпертонія. У дітей клініка супроводжується синдромом несправжнього передчасного статевого дозрівання за ізосексуальним типом у хлопчиків і гетеросексуальним – у дівчаток. Інколи клініка андростероми поєднується з явищами гіперкортицизму за типом синдрому Іценка-Кушинга.
Кортикоестрома. Пухлина кори наднирників з гіперпродукцією естрогенів зустрічається рідко. Описана у чоловіків і дітей обох статей, у дорослих жінок виявляють випадково, позаяк фемінізацію жінок клінічно виявити неможливо. У жінок кортикоестрому діагностують у разі її поєднання з ознаками синдрому Іценка-Кушинга. Клініка характеризується розвитком елементів фемінізації чоловіків: гінекомастія, зміна статури, припинення росту бороди і вусів, атрофія яєчок, імпотенція, олігоспермія, хоча розміри статевого члена і передміхурової залози залишаються нормальними; інколи гіпертонія, збільшення маси тіла, підвищена втомлюваність, депресія. Ці пухлини зазвичай великого розміру і легко пальпуються. Інколи кортикоестрома комбінується з іншими пухлинами кори надниркових залоз.
Альдостерома. Клініка пухлини характеризується артеріальною гіпертензією, тахікардією, м’язовою слабкістю (міастенія). Міастенія може бути виражена від легкої м’язової слабкості до тяжких псевдопаралітичних станів. Характерним є зниження концентраційної функції нирок, поліурія, полідипсія, ніктурія, гіпоізостенурія, пієлонефрити. Знижується толерантність до вуглеводів. Пацієнти скаржаться на головний біль, переважно у лобних долях, запаморочення, задишку. Інколи відмічають біль у попереку.
Інциденталоми наднирників. Хворі з гормонально не функціонуючими пухлинами приходять до лікаря зі скаргами на біль у животі, попереку, підребір’ї, зниження апетиту, апатію. З-поміж менш розповсюджених симптомів – втрата ваги, інколи – гематурія, варикоцеле і порушення ритму дихання. Частина гормонально неактивних («німих») пухлин не мають визначеної клінічної симптоматики. При значних розмірах ці пухлини можуть бути доступними для пальпації, викликати порушення з боку розташованих поруч органів, судин і нервів. АТ зазвичай у нормі.
Диагностика
Діагностику пухлин кори наднирників проводять у три етапи: аналіз анамнезу та клінічної картини захворювання; проведення основних спеціальних гормональних і додаткових лабораторних методів обстеження; топічна діагностика.
Основними в діагностиці є гормональні методи дослідження: визначення добової екскреції із сечею 11- та 17-оксикортикостероїдів (11- та 17-ОКС ), 17-кетостероїдів (17-КС), кортизолу; у крові – рівень АКТГ, кортизолу, ДЕА (ДЕА-с), тестостерону, 17-β-гідроксипрогестерону (17-β-ОН-Пр), альдостерону, реніну. До важливих належать також топічні методи діагностики: УЗД зачеревного простору, КТ і МРТ надниркових залоз та гіпофіза.
Алгоритм діагностики пухлин наднирників представлений на схемі 1. На першому етапі аналізу скарг пацієнта ендокринолог з’ясовує наявність характерних ознак гіперкортицизму (схема 2). Якщо виявляють дві й більше ознак гіперкортицизму (див. схему 2), то призначають додаткове гормональне і параклінічне обстеження (див. схему 1). Алгоритм діагностики синдрому Іценка-Кушинга представлений на схемі 3.
Обов’язкові лабораторні дослідження
Інструментальні та інші методи діагностики
Інструментальні та інші методи діагностики
Консультації суміжних спеціалістів
Обов’язкові: окуліста, кардіолога, невропатолога.
За наявності показань: гінеколога/андролога, нефролога, гастроентеролога, генетика.
Схема 1. Етапи діагностики пухлин наднирників
Схема 2. Клінічні синдроми і частота їх поширення при гіперкортицизмі
Схема 3. Алгоритм діагностики синдрому Іценка-Кушинга
Схема 4. Алгоритм діагностики та диференціальної діагностики андростероми
Схема 5. Діагностичний алгоритм синдрому альдостеронізму
У разі неповної клінічної картини і незначних змінах гормональних показників для підтвердження діагнозу проводять додаткові функціональні тести з метопіроном, дексаметазоном (малий і великий).
Методика проведення:
- Малий дексаметазоновий тест проводять в умовах стаціонару через добу після госпіталізації. Передбачається приймання дексаметазону по 0,5 мг кожні 6 год упродовж 2-х діб. До і після призначення дексаметазону визначають вміст 17-ОКС і 117-КС у добовій сечі та кортизолу в крові.
- Великий дексаметазоновий тест проводять після малого, якщо при проведенні останнього не відбувається достатнього зниження екскреції 17-ОКС і 17-КС та кортизолу в крові. При проведенні великого тесту дексаметазон призначають у дозі 2 мг кожні 6 год упродовж 2-х діб (8 мг/добу). До початку і після закінчення тесту досліджують вміст кортизолу в крові та 17-ОКС і 17-КС у добовій сечі.
- Пробу з метопіроном проводять з метою диференціальної діагностики хвороби і синдрому Іценка-Кушинга. До початку проведення проби визначають екскрецію 17-ОКС у добовій сечі, затим пацієнт приймає метопірон у дозі 500 мг кожні 4 год (загалом 6 разів). Після завершення проби знову визначають добову екскрецію 17-ОКС.
Пояснення результатів.
Дексаметазон є блокатором секреції АКТГ. У здорових осіб це призводить до пригнічення секреції кортикостероїдів наднирниками і відповідно до зменшення екскреції їх метаболітів.
- У хворих із гіпоталамічним синдромом й ознаками гіперкортицизму при проведенні малої проби екскреція 17-ОКС і рівень кортизолу в крові зменшуються порівняно з вихідними показниками у 2 рази і більше. Подібне не спостерігається за наявності ендогенного гіперкортицизму – хвороби Іценка-Кушинга чи синдрому Кушинга.
- У хворих із хворобою Іценка-Кушинга при проведенні великої проби з дексаметазоном також під впливом останнього пригнічується секреція АКТГ, а відповідно й екскреція 17-ОКС. Знижується також рівень кортизолу в крові, а при синдромі Кушинга (гормон-продукуюча пухлина наднирників) цього не відбувається.
- Метопірон пригнічує активність 11β-гідроксилази, що призводить до зниження секреції кортизолу, альдостерону і кортикостерону. Зменшення концентрації кортизолу в крові за механізмом «зворотного зв’язку» призводить до підвищення секреції АКТГ із наступною стимуляцією утворення КС. Однак у зв’язку з блокадою 11β-гідроксилази у великій кількості синтезуються тільки попередники кортизолу (17-гідрокси-11-дезоксикортикостерон, або S-речовина). При хворобі Іценка-Кушинга після призначення метопірону секреція 17-ОКС із сечею підвищується, а при синдромі Іценка-Кушинга вона не змінюється.
Примітки.
У практично здорових осіб екскреція 17-ОКС із сечею під впливом метопірону також підвищується до 28 мкмоль/добу, а при хворобі Іценка-Кушинга – більш виражено (28 мкмоль/добу).
При визначенні лише 17-ОКС інформативність проб не перевищує 45%. Визначення додатково й кортизолу плазми підвищує інформативність тесту до 60-70%. Ускладнень немає.
Диференційна діагностика
Диференціальну діагностику пухлин кори надниркових залоз проводять з хворобою Іценка-Кушинга, гіпоталамічним синдромом, ВДКН, склерополікістозом яєчників, деякими нозологічними формами вродженої патології статевих залоз, пубертатною гінекомастією, феохромоцитомою та іншими типами гіпертензій.
Диференціальну діагностику пухлин кори наднирників передусім проводять із хворобою Іценка-Кушинга й АКТГ-ектопованим синдромом.
Диференційна діагностика гіперкортицизму
Диференціація андростероми проводиться передусім із ВДКН (схема 4) і склерополікістозом яєчників, а також з пухлинами яєчників. Для цього обов’язково застосовують додаткове гормональне обстеження з проведенням спеціальних тестів (див. «Обов’язкові та додаткові лабораторні обстеження»; схема 4). При пухлинах яєчника (аренобластома та ін.), яким також притаманна вірилізація, екскреція 17-КС помірно підвищена, 17-ОН-прогестерон у нормі й підвищений рівень ДЕА в крові. У таких випадках потрібне додаткове обстеження гінеколога, УЗД і/чи МРТ органів малого таза.
У чоловіків пухлина яєчника, яка розвивається з клітин Лейдіга, проявляється клінікою андростероми, проте пальпаторно виявляється значне збільшення одного яєчка. 17-КС у добовій сечі при цьому підвищені помірно, а вільний тестостерон крові значно підвищений.
Варто зауважити, що деякі гепатоми, як правило злоякісні, можуть секретувати гонадотропіни і внаслідок цього призводити до появи ознак передчасного статевого розвитку та вірилізації. Збільшена печінка, підвищений рівень гонадотропінів і нормальна концентрація 17-ОН-прогестерону та ДЕА (ДЕА-с) у крові, нормальна екскреція 17-КС, 17-ОКС із сечею за добу допомагають правильній діагностиці.
Кортикоестроми диференціюють із синдромом Іщенка-Кушинга, пубертатною гінекомастією, гіпоталамічним синдромом, синдромом Клайнфельтера, оваріальними і тестикулярними естрогенпродукуючими пухлинами. Для цього визначають каріотип, рівень статевих гормонів і гонадотропінів, їх добовий ритм; проводять функціональні проби (див. «Обов’язкові та додаткові лабораторні обстеження», схеми 2 і 3), консультації суміжних спеціалістів. При синдромі Клайнфельтера, коли також спостерігається двобічна гінекомастія, під час проведення каріотипування лімфоцитів периферичної крові виявляється хромосомний набір 47, ХХV, у крові значно підвищений рівень гонадотропінів, а тестостерон знижений, що дає підставу для правильної діагностики. Гінекомастія зустрічається при тиреотоксикозі та захворюваннях печінки, при вживанні деяких лікарських препаратів: резерпін, наперстянка, мепробамат.
Помірна транзиторна гінекомастія зустрічається в підлітків, але додаткове гормональне обстеження не виявляє змін у цих показниках.
У разі підозри на альдостерому проводять диференціальну діагностику з синдромом Біглієри (дефект 17β-гідроксилази) та ін. Гіпертензивними формами адреногенітального синдрому – ВДКН, із феохромоцитомою (значне підвищення катехоламінів і ВМК у сечі та крові), глюкортикоїдною гіпертензією при синдромі Іценка-Кушинга (див. схеми 3 і 5), гіпертензією при гіпоталамічному синдромі, патології нирок, тиреотоксикозі (схема 5). Часто гіпертензія розвивається при довготривалому вживанні препаратів кореня солодки, ртутних паст і мазей тощо.
Лечение
Усі хворі з пухлинами наднирників, які мають ознаки гормональної активності чи злоякісного росту (дані КТ, МРТ), та пухлинами розміром понад 4 см потребують хірургічного втручання – адреналектомії. За наявності злоякісного росту також видалять паранефральну клітковину. За наявності інкурабельної пухлини можливе проведення емболізації судин, які постачають кров до пухлини, для зменшення темпів росту останньої та її гормональної активності. Операцію можуть відкласти у разі вираженої серцево-судинної недостатності, порушеннях мозкового чи коронарного кровообігу, тяжких порушеннях КЛС, електролітно-водного обміну та біохімічних і загальних аналізах сечі й крові до їх усунення.
При пухлинах наднирників без ознак гормональної активності та розміром до 4 см можливий нагляд з контролем росту кожні 6 міс. Якщо спостерігається розвиток пухлини, показано оперативне втручання.
При злоякісних пухлинах і пухлинах розміром понад 6 см проводять відкриту адреналектомію. Якщо пухлини меншого розміру, рекомендується проводити лапароскопічну адреналектомію.
Характеристика кінцевого очікуваного результату лікування
При лікуванні доброякісних гормонально неактивних пухлин хворі цілком виліковуються, працездатність зберігається.
При лікуванні доброякісних гормонально активних пухлин у результаті лікування досягається зворотний розвиток стероїдної кардіо- та енцефалопатії, стероїдного діабету, працездатність хворих буде залежати від тяжкості перебігу захворювання, кількості та тяжкості ускладнень (хворі можуть працювати лише за певних умов виробництва і за певним графіком). При злоякісних пухлинах наднирників після хірургічного лікування прогноз залежить від розповсюдженості процесу, агресивності пухлинного росту.
Рекомендації щодо подальшої, за необхідності, медичної допомоги хворому
Після хірургічного лікування хворі потребують ретельного диспансерного нагляду, проведення повного ендокринологічного обстеження кожні 6 міс.
Вимоги до режиму праці, відпочинку, лікування, реабілітації
Хворі після радикального хірургічного лікування повинні дотримуватися режиму праці (забороняється робота в нічні години або в гарячих цехах, перебування на сонці), роботу треба чергувати з відпочинком. Пацієнти потребують 8-годинного нічного сну. Профілактичні заходи і лікування мають бути неперервними, контрольованими й адекватними за тривалістю.
Форма інформованої згоди пацієнта на виконання протоколу
Додаткова інформація для пацієнта і членів його родини. Рекомендації ендокринологів щодо харчування, фізичної активності та санаторно-курортного лікування.
Методологія та критерії ефективності виконання протоколу.
Ендокринологи й онкологи поліклінік, диспансерів, центрів проводять ретельний облік хворих з виявленими новоутвореннями наднирників та хворих, які оперовані з приводу пухлин кори наднирників, слідкують за проведенням контрольних обстежень (кожні 6 міс). Окремо враховують осіб після тотальної адреналектомії з хронічною наднирниковою недостатністю і коригують замісну кортикостероїдну терапію. Принципи рандомізації не передбачені. Діагностику ускладнень і побічних ефектів лікування проводять за загальноприйнятими схемами. Порядок виключення пацієнта з моніторингу не передбачений. Параметри оцінки якості життя при виконанні протоколу передбачають, що досягнення повної клініко-гормональної ремісії уможливить збереження якості життя хворих і підвищить їх працездатність. Оцінку вартості виконання протоколу проводять планові відділи відповідних установ.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення

 Стандарти діагностики та лікування ендокринних захворювань. Пухлини коркового шару наднирників МКХ-10: D35.0, С74.0, E26.0
Стандарти діагностики та лікування ендокринних захворювань. Пухлини коркового шару наднирників МКХ-10: D35.0, С74.0, E26.0
 Вроджена дисфункція кори наднирників
Вроджена дисфункція кори наднирників
 Вазоренальна гіпертензія: сучасний стан проблеми
Вазоренальна гіпертензія: сучасний стан проблеми
 Бронхит рецидивирующий
Бронхит рецидивирующий