Такролимус 0,5 мг инструкция, аналоги и состав
| Показания: | Профілактика відторгнення алотрансплантата печінки, нирок та серця. Лікування відторгнення алотрансплантата, резистентного до стандартних режимів імуносупресивної терапії. |
| Форма випуска: | Капсули по 0,5 мг № 30 (10х3), № 60 (10х6) у блістерах |
| Производитель, страна: | Інтас Фармасьютікалс Лімітед, Індія |
| Действующее вещества: | 1 капсула містить такролімусу (у вигляді такролімусу моногідрату) 0,5 мг |
| МНН: | Tacrolimus - Такролимус |
| Регистрация: | UA/11791/01/01з 25.10.2011 по 25.10.2016. Приказ 693 від 25.10.2011 |
| Код АТХ: |
|
Склад:
діюча речовина:такролімус;
1 капсула містить такролімусу (у вигляді такролімусу моногідрату) 0,5 мг, або 1 мг, або 5 мг;
допоміжні речовини: лактози моногідрат, натрію кроскамерлоза, гіпромелоза, етанол безводний, магнію стеарат.
склад капсули: желатин, вода очищена, натрію лаурилсульфат, заліза оксид жовтий (Е 172), титану діоксид (Е 171).
Лікарська форма. Капсули.
Фармакотерапевтична група.
Імуносупресант. Інгібітор кальценеврину. Код АТС L04A D02.
Клінічні характеристики.
Показання.
Профілактика відторгнення алотрансплантата печінки, нирок та серця.
Лікування відторгнення алотрансплантата, резистентного до стандартних режимів імуносупресивної терапії.
Протипоказання.
Відома гіперчутливість до такролімусу (або до інших макролідів) та інших компонентів препарату. Дитячий вік до 6 років (для даної лікарської форми).
Спосіб застосування та дози.
Застосування такролімусу слід обмежувати спеціалізованими стаціонарними відділеннями та в амбулаторних умовах під контролем лікаря, який має досвід у призначенні імуносупресивної терапії після трансплантації.
Дозування препарату необхідно корегувати залежно від індивідуальних потреб пацієнта, враховуючи результати моніторингу рівнів препарату в крові.
Такролімус капсули застосовують перорально.
Такролімус зазвичай призначають з іншими імуносупресивними препаратами після трансплантації. Дозу такролімусу можна змінювати залежно від обраного режиму.
Рекомендується розподілити добову дозу препарату на два прийоми (наприклад, зранку та ввечері). Капсули слід приймати одразу ж після вилучення їх з блістерної упаковки. Капсули необхідно проковтнути, запиваючи рідиною (краще – водою). Для досягнення максимальної абсорбції препарат слід приймати на порожній шлунок (натще) або як мінімум за 1 годину до або 2 - 3 години після їди.
Тривалість лікування.
Тривалість лікування необмежена, оскільки імуносупресію слід підтримувати протягом тривалого періоду.
Трансплантація печінки
Первинна імуносупресію – дорослі.
Пероральну терапію Такролімусом необхідно розпочати з дози 0,1 - 0,2 мг/кг на добу, розподіливши цю дозу на два прийоми (наприклад, зранку та ввечері). Застосування препарату слід розпочинати приблизно через 12 годин після завершення операції.
Якщо стан пацієнта не дозволяє приймати препарат внутрішньо, проводять внутрішньовенну терапію такролімусом в іншій лікарській формі.
Первинна імуносупресія – діти віком від 6 років.
Рекомендовану початкову дозу препарату для перорального застосування 0,3 мг/кг на добу слід розподілити на два прийоми (зранку та ввечері). Якщо клінічний стан пацієнта не дозволяє приймати препарат внутрішньо, проводять внутрішньовенну терапію такролімусом в іншій лікарській формі.
Підтримуюча терапія – дорослі та діти віком від 6 років.
Дози Такролімусу зазвичай знижують під час підтримуючої терапії. У деяких випадках можливо відмінити препарати супутньої імуносупресивної терапії, залишивши Такролімус як монотерапію. Покращення стану пацієнта після трансплантації може змінити фармакокінетику такролімусу, тому виникає потреба в корекції дози препарату.
Лікування відторгнення – дорослі та діти віком від 6 років.
Для лікування епізодів відторгнення необхідно застосовувати вищі дози Такролімусу разом із додатковою кортикостероїдною терапією та короткими курсами введення моно/поліклональних антитіл. Якщо відзначаються ознаки токсичності, може виникнути необхідність у зниженні дози Такролімусу.
При переведенні пацієнтів на терапію Такролімусом рекомендуються ті самі початкові дози, як і при первинній імуносупресії. При переведенні пацієнтів з терапії циклоспорином на Такролімус необхідна інформація знаходиться в розділі «Особливості застосування»: перехід з терапії циклоспорином.
Трансплантація нирки
Первинна імуносупресія – дорослі.
Пероральну терапію Такролімусом необхідно розпочинати з дози 0,2 - 0,3 мг/кг на добу, розподіливши цю дозу на два прийоми (зранку та ввечері). Терапію препаратом слід розпочинати протягом 24 години після завершення операції.
Якщо стан пацієнта не дозволяє приймати препарат внутрішньо, проводять внутрішньовенну терапію такролімусом в іншій лікарській формі.
Первинна імуносупресія – діти віком від 6 років.
Пероральну терапію Такролімусом необхідно розпочинати з дози 0,3 мг/кг на добу, розподіливши цю дозу на два прийоми (зранку та ввечері). Якщо стан пацієнта не дозволяє приймати препарат внутрішньо, проводять внутрішньовенну терапію такролімусом в іншій лікарській формі.
Підтримуюча терапія – дорослі та діти віком від 6 років.
Дози Такролімусу зазвичай знижують під час підтримуючої терапії. У деяких випадках можливо відмінити препарати супутньої імуносупресивної терапії, залишивши Такролімус у якості базової терапії. Поліпшення стану пацієнта після трансплантації може змінити фармакокінетику такролімусу, тому виникає потреба в корекції дози препарату.
Лікування реакції відторгнення – дорослі та діти віком від 6 років.
Для лікування епізодів відторгнення необхідно застосовувати вищі дози Такролімусу разом із додатковою кортикостероїдною терапією та короткими курсами введення моно/поліклональних антитіл. Якщо відзначаються ознаки токсичності, може виникнути необхідність у зниженні дози Такролімусу.
При переведенні пацієнтів на терапію Такролімусом рекомендуються ті самі початкові дози, як і при первинній імуносупресії. При переведенні пацієнтів з терапії циклоспорином на Такролімус необхідна інформація знаходиться в розділі «Особливості застосування»: перехід з терапії циклоспорином.
Трансплантація серця
Первинна імуносупресія – дорослі.
Такролімус можна застосовувати разом з індукцією антитілами (з урахуванням відтермінування початку лікування Такролімусом) або без призначення антитіл у клінічно стабільних хворих.
Після індукції антитілами пероральну терапію Такролімусом необхідно розпочинати з дозування 0,075 мг/кг на добу, розподіливши цю дозу на два приймання (наприклад, зранку та ввечері). Застосування препарату слід розпочинати протягом 5 діб після завершення операції, як тільки стабілізується клінічний стан хворого. Якщо стан пацієнта не дозволяє приймати препарат внутрішньо, проводять терапію такролімусом в іншій лікарській формі.
Існує опублікований альтернативний підхід, при якому пероральний прийом такролімусу розпочинається протягом 12 годин після трансплантації. Цей підхід призначений для пацієнтів без ознак порушень функції внутрішніх органів (наприклад, нирки). У цьому випадку такролімус у початковій дозі 2 - 4 мг на добу комбінується з мікофенолату мофетилом та кортикостероїдами або сиролімусом та кортикостероїдами.
Первинна імуносупресія – діти віком від 6 років.
Після трансплантації серця у дітей первинну імуносупресію Такролімусом можна проводити як разом з індукцією антитілами, так і самостійно.
У випадках, коли індукція антитілами не проводиться, Такролімус вводиться в іншій лікарській формі внутрішньовенно до досягнення концентрації такролімусу в нерозведеній крові 15 - 25 нг/мл.
При першій же клінічній можливості необхідно перевести пацієнта на пероральний прийом Такролімусу. Початкова рекомендована доза становить 0,3 мг/кг на добу, яку призначають через 8 -12 годин після закінчення внутрішньовенної інфузії.
Після індукції антитілами пероральну терапію Такролімусом необхідно розпочинати з дози 0,1 - 0,3 мг/кг на добу, розподіливши цю дозу на два прийоми (зранку та ввечері).
Підтримуюча терапія – дорослі та діти віком від 6 років.
Дози Такролімусу зазвичай знижують під час підтримуючої терапії. Поліпшення стану пацієнта після трансплантації може змінити фармакокінетику такролімусу, тому виникає потреба в корекції дози препарату.
Лікування відторгнення – дорослі та діти віком від 6 років.
Для лікування епізодів відторгнення необхідно застосовувати вищі дози Такролімусу разом із додатковою кортикостероїдною терапією та короткими курсами введення моно/поліклональних антитіл.
При переведенні дорослих пацієнтів на терапію Такролімусом початкову дозу препарату 0,15 мг/кг на добу слід розподілити на два прийоми (зранку та ввечері).
При переведенні дітей на терапію Такролімусом початкову дозу препарату 0,2 - 0,3 мг/кг на добу слід розподілити на два прийоми (зранку та ввечері).
Інформація щодо переведення пацієнтів з терапії циклоспорином на Такролімус викладена в розділі «Особливості застосування»: перехід з терапії циклоспорином.
Рекомендовані дози після алотрансплантації інших органів.
Клінічний досвід застосування Такролімусу пацієнтам після алотрансплантації легені, підшлункової залози та кишки обмежений. Після трансплантації легені Такролімус застосовують у початковій дозі 0,1 - 0,15 мг/кг на добу, алотрансплантації підшлункової залози – в початковій дозі 0,2 мг/кг на добу. У пацієнтів після алотрансплантації кишки початкова доза становить 0,3 мг/кг на добу.
Для досягнення подібних рівнів препарату в крові дітям зазвичай потрібні дозування в 1,5 - 2 рази вищі, ніж дорослим.
Рекомендовані дози для пацієнтів з печінковою недостатністю.
Дози Такролімусу можна знижувати пацієнтам з печінковою недостатністю для підтримання рівня препарату в плазмі крові в рамках градацій, що рекомендуються.
Рекомендовані дози для пацієнтів з нирковою недостатністю.
Оскільки фармакокінетика такролімусу не змінюється залежно від функції нирок, коригування дози не потрібно. Однак у зв’язку з наявністю у такролімусу нефротоксичної дії рекомендується ретельно контролювати функцію нирок (у тому числі концентрацію креатиніну в сироватці крові, кліренс креатиніну та рівень діурезу).
Рекомендовані дози для пацієнтів літнього віку.
У даний час відсутні дані щодо необхідності коригування дози для пацієнтів літнього віку.
Побічні реакції.
Побічні реакції препарату, пов’язані з імунодепресивними препаратами, часто важко визначити внаслідок основного захворювання та паралельного застосування супутнього лікування.
Більшість із наведених нижче небажаних реакцій оборотні та/або зменшуються при зниженні дозування. При пероральному прийманні такролімусу частота розвитку небажаних реакцій нижча, ніж при внутрішньовенному введенні. Побічні реакції такролімусу наведені нижче в порядку, залежному від частоти розвитку:
Дуже часто (> 1/10); часто (> 1/100 < 1/10); іноді (> 1/1000 < 1/100); рідко (> 1/10000 < 1/1000); дуже рідко (< 1/10000, у тому числі поодинокі випадки).
Інфекції та інвазії
Як і при лікуванні іншими імуносупресивними препаратами, пацієнти, які отримують такролімус, мають підвищений ризик розвитку інфекційних захворювань (вірусних, бактеріальних, грибкових, протозойних). Може погіршитись перебіг раніше діагностованих інфекційних захворювань. Також можуть виникнути локалізовані інфекції.
Новоутворення
Пацієнти, які отримували імуносупресивну терапію, входять до групи підвищеного ризику розвитку злоякісних пухлин. При застосуванні такролімусу відзначено розвиток як доброякісних, так і злоякісних пухлин, у тому числі вірусу Епштейн-Барр – асоційованих (EBV) лімфопроліферативних захворювань та раку шкіри.
З боку крові та лімфатичної системи
Часто: анемія, лейкопенія, тромбоцитопенія, геморагія, лейкоцитоз, порушення коагуляції.
Іноді: коагулопатія, викривлення результатів дослідження коагуляції та аналізів крові, панцитопенія, тромботична мікроангіопатія.
Рідко: тромбоцитопенічна пурпура, гіпопротеїнемія.
Реакції гіперчутливості
У пацієнтів, які отримують такролімус, були відзначені алергічні та анафілактичні реакції.
З боку ендокринної системи
Рідко: гірсутизм.
Метаболізм та електроліти
Дуже часто: гіперглікемія, гіперкаліємія, цукровий діабет.
Часто: гіпомагніємія, гіперліпідемія, гіперхолестеринемія, гіпертригліцеридемія, гіпофосфатемія, гіпокаліємія, гіперурикемія, гіпокальціємія, метаболічний ацидоз, гіпонатріємія, гіперурикемія, гіповолемія, інші порушення електролітного балансу.
Іноді: дегідратація, гіпопротеїнемія, гіперфосфатемія, гіпоглікемія.
Психічні порушення
Дуже часто: безсоння.
Часто: тривожність, нервозність, порушення сну, порушення свідомості, емоційна лабільність, галюцинації.
Іноді: психічні порушення.
З боку нервової системи
Дуже часто: тремор, головний біль.
Часто: порушення чутливості (наприклад, парестезія), сплутаність свідомості, депресія, запаморочення, збудження, нейропатія, судоми, дискоординація, психоз, отологічні порушення, енцефалопатія.
Іноді: підвищення м`язового тонусу, захворювання очей, амнезія, катаракта, порушення мови, параліч, кома, глухота.
Рідко: гіпертонія.
Дуже рідко: міастенія.
З боку органа зору
Часто: зорові порушення, фоточутливість.
Іноді: катаракта.
Рідко: сліпота.
З боку органа слуху
Часто: дзвін у вухах.
Іноді: гіпоакузія.
Рідко: нейросенсорна глухота.
З боку серцево-судинної системи
Часто: ішемія коронарних судин, тахікардія, гіпертензія.
Іноді: шлуночкові аритмії, зупинка серця, кардіоміопатія, шлуночкова гіпертрофія, надшлуночкові аритмії, фібриляція, відхилення в параметрах Ехо-КГ, серцева недостатність, крововиливи, прояви ішемії та тромбоемболії, периферичні судинні порушення.
Рідко: перикардіальний випіт, інфаркт, тромбоз глибоких вен, шок.
Дуже рідко: відхилення в параметрах Ехо-КГ.
З боку дихальної системи
Часто: порушення респіраторної функції (наприклад, задишка), плевральний випіт, диспное, фарингіт, кашель.
Іноді: порушення дихання, ателектазія, астма.
Рідко: респіраторний дистрес-синдром.
З боку системи травлення
Дуже часто: діарея, нудота та/або блювання.
Часто: дисфункція ШКТ (наприклад, диспепсія), біль у животі, запор, зміна ваги та апетиту, запалення та виразки в ШКТ, шлунково-кишкові крововиливи, метеоризм.
Іноді: асцит, кишкова непрохідність, перитоніт, підвищення амілази в крові, панкреатит.
Рідко: субілеус, панкреатичні псевдокісти.
З боку жовчовивідних шляхів
Часто: відхилення в рівнях ферментів печінки, жовтяниця, захворювання жовчних шляхів та жовчного міхура, ураження тканини печінки, гепатит.
Рідко: тромбоз артерій печінки, оклюзія печінкових судин.
Дуже рідко: печінкова недостатність, стеноз жовчної протоки.
З боку шкіри
Часто: свербіж, алопеція, висипання, підвищена пітливість, акне.
Іноді: дерматит, фоточутливість.
Рідко: синдром Лайєлла.
Дуже рідко: синдром Стівенса-Джонсона.
З боку скелетно-м’язової системи
Часто: артралгія, м’язові спазми, біль у кінцівках та попереку, судоми.
Іноді: міастенія, захворювання суглобів.
З боку ниркової системи
Дуже часто: порушення функції нирок (наприклад, підвищення рівня креатиніну в сироватці крові).
Часто: ураження тканини нирок, гостра ниркова недостатність, олігурія, нирково-канальцевий некроз, токсична нефропатія.
Іноді: анурія, гемолітичний уремічний синдром.
З боку репродуктивної системи
Іноді: дисменорея, маткова кровотеча.
Загальні прояви
Часто: астенія, лихоманка, набряки, біль та дискомфорт, кровотеча, жар, підвищення маси тіла.
Іноді: мультиорганні порушення, грипоподібний синдром, нервозність, зниження ваги тіла.
Рідко: спрага, почуття тиску у грудях, зменшення рухливості.
Дуже рідко: збільшення маси жирової тканини.
У поодиноких випадках спостерігався розвиток гіпертрофії шлуночка або гіпертрофії міжшлуночкової перегородки серця, зареєстрованих як кардіоміопатії. У більшості випадків ці прояви були оборотними, розвиваючись в основному у дітей, у яких мінімальні концентрації такролімусу в крові набагато перевищували рекомендовані максимальні рівні. Іншими факторами, які підвищують ризик розвитку таких клінічних станів, були: раніше існуючі захворювання серця, застосування кортикостероїдів, гіпертензія, дисфункції нирок або печінки, інфекції, надлишок рідини в організмі та набряки.
Передозування.
Клінічний досвід лікування передозування обмежений. Відзначено кілька випадків випадкового передозування препарату, при цьому спостерігались такі симптоми: тремор, головний біль, нудота, блювання, інфекції, кропив’янка, летаргія, збільшення рівня азоту сечовини крові та підвищення сироваткових концентрацій креатиніну, збільшення рівнів аланін амінотрансферази.
Специфічний антидот до Такролімусу відсутній. Якщо з’явилися симптоми передозування, необхідно прийняти стандартні засоби підтримки та провести симптоматичне лікування.
У зв’язку з високою молекулярною вагою, поганою розчинністю у воді та зв’язуванням з еритроцитами та білками плазми крові значною мірою очікується, що при передозуванні такролімусу діаліз не буде ефективним. У окремих хворих з дуже високими рівнями препарату в плазмі крові гемофільтрація та діафільтрація виявились ефективними, знижуючи токсичні концентрації препарату. У випадках розвитку інтоксикації після перорального застосування препарату може допомогти промивання шлунка та/або приймання адсорбентів (таких як активоване вугілля).
Застосування у період вагітності або годування груддю.
Оскільки такролімус може впливати на метаболізм стероїдних контрацептивів, особливу увагу слід приділити запобіганню вагітності.
Препарат може проникати крізь плаценту. Оскільки безпечність застосування Такролімусу вагітним жінкам не встановлена, не слід призначати цей препарат вагітним жінкам, за винятком випадків, коли отримана користь від лікування виправдовує потенційний ризик для плода.
Такролімус виділяється з грудним молоком. Оскільки не можна виключити негативний вплив на немовлят, жінкам, які приймають препарат, слід припинити годування груддю.
Діти.
У даній лікарській формі застосовують препарат у дітей віком від 6 років.
Особливості застосування.
Результати аналізу клінічних випробувань дають змогу припустити, що можна успішно проводити лікування більшості пацієнтів, якщо мінімальні рівні такролімусу в крові підтримуються нижче 20 нг/мл. Інтерпретуючи дані щодо концентрації препарату в нерозведеній крові, важливо оцінювати клінічний стан пацієнта.
У клінічній практиці протягом раннього періоду після проведення трансплантації мінімальні рівні препарату в нерозведеній крові зазвичай коливались у межах 5-20 нг/мл після трансплантації печінки та 10-20 нг/мл після трансплантації нирки і серця. Надалі під час підтримуючої терапії після трансплантації печінки, нирки і серця концентрації препарату в крові варіюють від 5 до 15 нг/мл.
Протягом початкового періоду після проведення трансплантації необхідно проводити моніторинг таких параметрів: артеріальний тиск, Ехо-КГ, неврологічний та візуальний статус, рівні глюкози в крові натще, електроліти (особливо калій), функцію печінки та нирок, параметри клінічного аналізу крові, показники коагуляції та визначення білків у плазмі крові.
Фітопрепарати, що мають у своєму складі звіробій (Hypericum perforatum) та інші трав’яні збори, необхідно виключити протягом терапії такролімусом через можливу взаємодію, що веде до зниження такролімусу у плазмі крові та зменшення клінічного ефекту терапії.
Оскільки концентрація такролімусу у плазмі крові може значно змінитися під час виникнення епізодів діареї, необхідний додатковий контроль концентрації Такролімусу протягом епізодів діареї.
Як і при застосуванні інших імуносупресивних препаратів, внаслідок потенційного ризику розвитку злоякісних змін шкіри слід обмежити вплив сонячних променів та УФ-випромінювання, захищаючи шкіру одягом та використовуючи креми з високим фактором захисту.
У дітей ( у віці від 2 років) с EBV- серонегативною реакцією відзначається підвищений ризик розвитку лімфопроліферативних захворювань (для цієї групи пацієнтів до початку застосування Такролімусу необхідно серологічне визначення вірусу EBV).
Перехід з терапії циклоспорином. Необхідно з особливою обережністю переводити пацієнтів з циклоспорину на терапію Такролімусом. Оскільки супутнє застосування циклоспорину та Такролімусу може збільшити період напіввиведення циклоспорину та підсилити токсичні ефекти, лікування Такролімусом слід розпочинати після оцінки концентрацій циклоспорину в крові хворого та клінічного стану пацієнта. Застосування препарату слід відкласти при наявності підвищених рівнів циклоспорину в крові хворого. На практиці лікування Такролімусом розпочиналось через 12-24 години після припинення прийому циклоспорину. Після переведення пацієнта необхідно продовжувати моніторинг рівнів циклоспорину у крові хворого у зв’язку з можливістю порушення в кліренсі циклоспорину.
Рекомендації щодо досягнення необхідного рівня концентрації препарату в нерозведеній крові.
Вибір дозування препарату має базуватися на результатах клінічної оцінки процесу відторгнення та перенесення препарату кожним пацієнтом індивідуально. З метою оптимізації дозування препарату використовується визначення концентрації Такролімусу в нерозведеній крові за допомогою імунних методів, включаючи напівавтоматичний імуноферментний аналіз на мікрочастинках (МІФА). Порівняння даних щодо концентрації Такролімусу в крові, які опубліковані в літературі, з індивідуальними клінічними показниками необхідно проводити з обережністю і на підставі знань та розуміння методу оцінки, що застосовувався.
У ранньому періоді після операції слід контролювати мінімальні рівні Такролімусу в нерозведеній крові.
Під час застосування такролімусу ефективність вакцин зменшується, і слід уникати введення живих атенуйованих вакцин.
Протягом терапії такролімусом, як і іншими імунодепресивними препаратами, немає даних щодо можливого ризику розвитку вторинного раку.
Пацієнтам, які мають рідкісні спадкові проблеми непереносимості галактози чи порушення глюкозогалактозної мальабсорбції, не слід застосовувати препарат.
Такролімус несумісний з полівінілхлоридом (PVC). Якщо вміст капсул необхідно вводити через назогастральний зонд, останній не повинен містити полівінілхлорид.
Здатність впливати на швидкість реакції при керуванні автотранспортом або роботі з іншими механізмами.
Слід утримуватися від керування автомобілем або роботі з механізмами.
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Метаболічні взаємодії. Такролімус метаболізується переважно печінковим мікросомальним цитохромом Р4503А4 ізоензимом (CYP3A4). Одночасне застосування лікарських або рослинних препаратів, які інгібують або індукують CYP3A4, може вплинути на метаболізм такролімусу, і таким чином знизити або підвищити рівні такролімусу в крові, тому необхідний додатковий контроль концентрації такролімусу протягом такого періоду.
Такролімус також впливає на CYP3A4 залежний метаболізм; таким чином, одночасне застосування такролімусу з препаратами, які метаболізуються CYP3A4 залежними шляхами, може вплинути на метаболізм цих препаратів (наприклад, кортизон, тестостерон).
Інгібітори метаболізму
Нижченаведені препарати індукують CYP3A4 та підвищують рівні такролімусу в крові:
- сильну взаємодію мають протигрибкові препарати, такі як кетоконазол, флюконазол, ітраконазол, клотримазол, вориконазол, макролідні антибіотики (еритроміцин) та інгібітори ВІЛ протеаз. Тому одночасне застосування цих речовин може потребувати зниження дози такролімусу практично у всіх пацієнтів.
- слабшу взаємодію мають клотримазол, кларитроміцин, джозаміцин, ніфедипін, нікардипін, дилтіазем, верапаміл, даназол, етинілестрадіол, омепразол та нефазодон.
- на підставі результатів досліджень in vitro такі речовини можна розглядати як потенційні інгібітори метаболізму: бромокриптин, кортизон, дапсон, ерготамін, ерготамін, ксикаїн, гестоден, лідокаїн, мефенітоїн, міконазол, мідазолам, нілвадипін, поретидрон, квінідин, тамоксифен, олеандоміцин.
Відзначено, що грейпфрутовий сік підвищує рівень такролімусу в крові внаслідок інгібування активності CYP3A4.
Індуктори метаболізму
Нижченаведені препарати індукують CYP3A4 та знижують рівні такролімусу в крові:
- сильну взаємодію мають рифампіцин, фенітоїн або звіробій (Hypericumperforatum), супутнє застосування якого може потребувати підвищення дози такролімусу практично всім пацієнтам. Клінічно суттєва взаємодія існує також з фенобарбіталом.
Під час супутнього застосування кортикостероїдів у потрібних для лікування дозах відзначалося зниження концентрації такролімусу в плазмі крові. Відзначено, що метилпреднізолон як підвищував, так і знижував рівні такролімусу в плазмі крові.
На основі результатів досліджень такі речовини як карбамазепін, метамізол та ізоніазид можна розглядати як потенційні індуктори цитохрому Р450 3А.
Період напіввиведення циклоспорину підвищувався при одночасному застосуванні з такролімусом. Крім того, можуть розвиватися синергічні/адитивні ефекти нефротоксичності. Враховуючи ці причини, не рекомендується комбіноване застосування циклоспорину та такролімусу при призначенні такролімусу пацієнтам, які раніше отримували циклоспорин.
Такролімус може підвищувати рівень фенітоїну в плазмі крові.
Доступні лише обмежені дані щодо взаємодії такролімусу зі статинами. Фармакокінетика статинів значною мірою не змінювалася під час супутнього застосування такролімусу.
Супутнє застосування такролімусу з препаратами, які мають нефротоксичні або нейротоксичні ефекти, може підвищити рівень токсичності (наприклад, аміноглікозиди, інгібітори гірази (ДНК-топоізомераза II роду), ванкоміцин, котримоксазол, нестероїдні протизапальні засоби, ганцикловір або ацикловір).
Підвищення нефротоксичності було отримано після застосування амфотерицину В та ібупрофену сумісно з такролімусом.
Оскільки лікування такролімусом може супроводжуватись розвитком гіперкаліємії або може підсилити раніше існуючу гіперкаліємію, слід уникати надлишкового прийому калію, застосування калійзберігаючих діуретиків (наприклад, амілорид, триамтерен або спіронолактон).
Такролімус значною мірою зв’язується з білками плазми крові. Слід врахувати можливі взаємодії з іншими препаратами, які є високо афінними до білків крові (наприклад, нестероїдні протизапальні засоби, пероральні антикоагулянти або пероральні протидіабетичні препарати).
Фармакологічні властивості.
Фармакодинаміка. На молекулярному рівні ефекти такролімусу зумовлюються зв’язуванням з цитозольним білком (FKBP12), який відповідає за внутрішньоклітинну акумуляцію препарату. Комплекс FKBP12-такролімус специфічно та конкурентно зв’язується з кальциневрином та інгібує його, що призводить до кальційзалежного інгібування Т-клітинних сигнальних шляхів трансдукції, таким чином запобігає транскрипції дискретної групи лімфокінних генів.
Такролімус являє собою високоактивний імуносупресивний препарат, який пригнічує формування цитотоксичних лімфоцитів, які в основному відповідають за відторгнення трансплантату, знижують активацію Т-клітин, залежну від Т-хелперів проліферацію В-клітин, а також формування лімфокінів (таких як інтерлейкіни-2, -3 та g-інтерферон), експресію рецептора інтерлейкіну-2.
Фармакокінетика.
Абсорбція. Такролімус абсорбується з усієї поверхні травного тракту.
Після перорального застосування концентрації (Сmах) такролімусу в крові досягають піку приблизно через 1-3 години. У деяких пацієнтів препарат абсорбується протягом тривалого періоду, досягаючи відносно рівного профілю абсорбції. Середнє значення параметрів абсорбції знаходиться в діапазоні 20-25 %.
Після перорального застосування (0,30 мг/кг/добу) препарату пацієнтами з трансплантатом печінки у більшості хворих рівноважні концентрації Такролімусу досягались протягом 3 днів.
У пацієнтів з трансплантатом печінки у стабільному стані біодоступність Такролімусу знижувалась при пероральному застосуванні препарату після вживання їжі з помірним вмістом жирів. Ефект від їжі з переважним вмістом вуглеводів був менш виражений.
У пацієнтів зі стабільним трансплантатом печінки відзначено біонакопичення такролімусу після вживання їжі з помірним вмістом жирів (34 % калорій).
Було відзначено також зниження площі під фармакокінетичною кривою AUC (27 %), максимальної концентрації Сmах (50 %) та збільшення tmaх (173 %) у нерозведеній крові. При одночасному застосуванні препарату з їжею знижувалася швидкість та ступінь абсорбції Такролімусу. Виділення жовчі не впливає на абсорбцію Такролімусу.
Спостерігається сильна кореляція між AUC (площі під кривою концентрація/час) та мінімальними рівнями препарату в нерозведеній крові при досягненні рівноважного стану, у зв’язку з цим моніторинг мінімальних рівнів препарату в нерозведеній крові може допомогти в адекватній оцінці системного впливу препарату.
Розподіл. У системному кровотоці такролімус значною мірою зв’язується з еритроцитами. Співвідношення нерозведена кров/плазмова концентрація становить близько 20:1. У плазмі крові препарат значною мірою зв’язується (> 98,8 %) з білками, в основному із сироватковими альбуміном та a-1-кислим глікопротеїном.
Такролімус широко розподіляється в організмі. Рівноважний об’єм розподілу на основі плазмових концентрацій становить приблизно 1 300 л (здорові добровольці). Відповідний показник на основі нерозведеної крові в середньому становить 47,6 л.
Такролімус – препарат з низьким рівнем кліренсу. Середнє значення загального кліренсу, який оцінюється за концентраціями препарату в нерозведеній крові, становить 2,25 л/годину. У дорослих пацієнтів з трансплантатом печінки і нирок значення цього параметру становили 4,1 л/годину та 6,7 л/годину відповідно. У дітей з трансплантатом печінки значення загального кліренсу приблизно в 2 рази вище, ніж у дорослих хворих із трансплантатом печінки.
Період напіввиведення такролімусу є тривалим та змінним. Середнє значення періоду напіввиведення з нерозведеної крові становить приблизно 43 години. У дорослих пацієнтів та дітей з трансплантатом печінки період напіввиведення в середньому становить 11,7 години та 12,4 години відповідно порівняно з 15,6 годинами у дорослих пацієнтів з трансплантатом нирки.
Метаболізм. Такролімус переважно метаболізується печінковим мікросомальним цитохромом Р4503А4 ізоензимом (CYP3A4). Такролімус значною мірою всмоктується у кишечнику. При використанні in vitro моделей виявлені вісім метаболітів, серед яких тільки один метаболіт має істотну імуносупресивну активність.
Виділення. Після перорального введення такролімусу, міченого 14С ізотопом, більшість радіоактивноміченого препарату виводилася з фекаліями. Приблизно 2 % виводиться з сечею. Менше 1 % незміненого такролімусу було виявлено в сечі та фекаліях, що вказує на те, що такролімус практично повністю метаболізується до елімінації. Основним шляхом елімінації є жовч.
Фармацевтичні характеристики.
Основні фізико-хімічні властивості:
капсули 0,5 мг – тверді желатинові капсули світло-жовтого кольору, з написом «5» на кришечці та корпусі, що містить порошок від білого до практично білого кольору;
капсули 1 мг – тверді желатинові капсули білого кольору, з написом «5» на кришечці та корпусі, що містить порошок від білого до практично білого кольору;
капсули 5 мг – тверді желатинові капсули рожевого кольору, з написом «4» на кришечці та корпусі, що містить порошок від білого до практично білого кольору.
Термін придатності.
2 роки.
Умови зберігання.
При температурі не вище 25 °С, в сухому, захищеному від світла та недоступному для дітей місці.
Упаковка.
10 капсул у блістері, 3 або 6 блістерів у картонній пачці.
Категорія відпуску.
За рецептом.
Виробник.
Інтас Фармасьютікалс Лімітед, Індія.
Місцезнаходження.
Плот № 457.458 с. Матода, вул. Балва Тал. Сананд штат Ахмадабад, 382 210 Гуджарат Індія.
Аналоги
Совпадает код ATХ + действующие вещества + форма випуска
| Международное название | Tacrolimus - Такролимус |
| Код АТХ | L04AD02 |
| Форма выпуска | капсулы |
- ПРОГРАФ® Астеллас Ірланд Ко., Лтд, Ірландія
- ПРОГРАФ® Астеллас Ірланд Ко., Лтд, Ірландія
- ПРОГРАФ® Астеллас Ірланд Ко., Лтд, Ірландія
- АДВАГРАФ® Астеллас Ірландія Ко., Лтд., Ірландія
- АДВАГРАФ® Астеллас Ірландія Ко., Лтд., Ірландія
- АДВАГРАФ® Астеллас Ірландія Ко., Лтд., Ірландія
- АДВАГРАФ® Астеллас Ірландія Ко., Лтд., Ірландія
- Такни 0,5 мг Лабораторіез Цинфа С.А., Іспанія
- Такни 1 мг Лабораторіез Цинфа С.А., Іспанія
- Такни 5 мг Лабораторіез Цинфа С.А., Іспанія
- Такролимус 1 мг Інтас Фармасьютікалс Лімітед, Індія
- Такролимус 5 мг Інтас Фармасьютікалс Лімітед, Індія

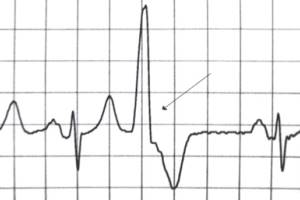 Клінічне значення та лікування шлуночкової екстрасистолії
Клінічне значення та лікування шлуночкової екстрасистолії
 Рекомендовані схеми діагностики та лікування пацієнтів з некоронарогенними хворобами та вадами серця
Рекомендовані схеми діагностики та лікування пацієнтів з некоронарогенними хворобами та вадами серця
 Що потрібно робити, щоб взнати стан свого серця і судин
Що потрібно робити, щоб взнати стан свого серця і судин
 Липразид — клинико-фармакологическая активность (укр)
Липразид — клинико-фармакологическая активность (укр)