- Головна
- /
- Статті
- /
- Ендокринологія. Цукровий діабет
- /
- Cиндром множинних ендокринних пухлин неоплазій
Cиндром множинних ендокринних пухлин неоплазій
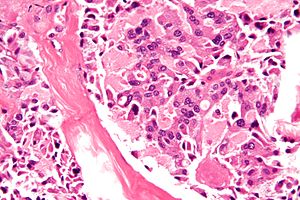
Під терміном «синдром множинних ендокринних пухлин (або неоплазій)» (МЕН) об’єднують захворювання, при яких виявляються пухлини нейроендокринного походження і/або гіперплазії (дифузні, вузликові) в двох або більше ендокринних органах.
МКХ-10: С73, D35.0
Загальна інформація
Основні риси синдромів МЕН:
- Різноманітні ендокринні та метаболічні порушення.
- Симптоми, зумовлені порушеннями секреції одного або декількох гормонів.
- Більшість пухлин має нейроендоектодермальне походження, вони часто злоякісні.
- Нерідко синдроми МЕН супроводжуються дисплазією інших органів і тканин.
- Як правило, в кожній ендокринній залозі є декілька вогнищ гіперплазії або пухлинного росту.
- Як спорадичні, так і сімейні випадки МЕН зумовлені генетичними дефектами і успадковуються аутосомно-домінантним шляхом.
- Виявлена чітка залежність клініко-лабораторних показників від стадії розвитку пухлини.
Етіологія і патогенез
У половині випадків МЕН виникають спорадично, тобто зумовлені мутацією, яка тільки-но з’явилася в статевих або соматичних клітинах. Ризик, що дитина хворого зі спорадичною формою МЕН захворіє, становить 50%. В сім’ях з МЕН-синдромом ризик захворювання дитини перевищує 75%. Таким чином, всі МЕН-синдроми характеризуються високою пенетрантністю.
Пухлини, характерні для синдромів МЕН, походять з клітин АПУД-системи, всі клітини АПУД є похідними від клітин нейроендоектодерми. Вважають, що синдроми МЕН зумовлені мутаціями в клітинах нервового гребінця. Причиною синдрому МЕН-1 служать мутації гена-супресора пухлинного росту (11q13). Цей ген кодує білок менін, який регулює проліферацію клітин-похідних нервового гребінця. Розвиток синдромів МЕН-2 пов’язаний із виникненням мутацій в RET-протоонкогені, який локалізується на довгому плечі 10-ї хромосоми.
Синдроми МЕН класифікують за основними клінічними проявами. Найпоширеніші компоненти цих синдромів подані в таблиці 1.
Клінічна картина
Синдром МЕН 1 типу
Частіше проявляється у віці 10-40 років, але описані поодинокі випадки розвитку даного синдрому і до 10 років. Першим проявом синдрому зазвичай є гіперпаратиреоз, який зустрічається у 90-95% випадків з синдромом і зумовлений гіперплазією прищитоподібних залоз.
Пухлини аденогіпофізу зустрічаються в 50-55% випадків, зазвичай гормонально неактивні. Характеризуються швидким ростом, що призводить до руйнування гіпофізу і розвитку пангіпопітуїтаризму. Якщо пухлина гормонально активна, то в клінічній картині спостерігаються ознаки, характерні для надлишку одного з гормонів:
- пролактинома – галакторея і аменорея;
- соматотропінома – акромегалія або гігантизм;
- кортикотропінома – синдром Іценка-Кушинга і гіперпігментація;
- тиротропінома – тиреотоксикоз;
- ЛГ- і ФСГ-секретуючі аденоми ведуть до фемінізації або маскулінізації.
Пухлини з острівцевих клітин спостерігаються у 50% випадків. Найпоширеніші варіанти – інсулінома, глюкагонома, гастринома і віпома (БТМС 2001). Симптом інсуліноми – гіпоглікемія, глюкагономи – гіперглікемія і некротична мігруюча еритема. Гастриноми проявляються синдромом Золінгера-Елісона (виразкова хвороба та інші порушення ШКТ). Віпома проявляється як панкреатична холера (водянисті випорожнення, гіпокаліємія, ахлоргідрія, метаболічний ацидоз).
Пухлини наднирників.
У 40% хворих виявляється гіперплазія або аденома наднирників. Гіперсекреції глюкокортикоїдів зазвичай немає, гіперплазія або аденома наднирників, як правило, є випадковою знахідкою при УЗД, КТ або МРТ.
Захворювання щитоподібної залози зустрічаються в 20% випадків у вигляді аденоми або раку щитовидної залози (не медулярного).
МЕН-2 синдроми
Синдром МЕН-2 включає три клінічні варіанти: синдром МЕН-2А, МЕН-2В, сімейна медулярна тиреоїдна карцинома.
Практично у всіх пацієнтів з МЕН-2А та МЕН-2В або ж сімейною медулярною карциномою щитовидної залози (СМКЩЗ) розвивається МКЩЗ. Приблизно 50% пацієнтів з МЕН-2А та МЕН-2В захворіють на феохромоцитому, 1/3 пацієнтів з МЕН-2А синдромом страждатимуть на гіперплазію паращитовидних залоз. Медулярна карцинома щитовидної залози, як правило, проявляється раніше, ніж інші компоненти МЕН-2А та МЕН-2В синдромів. Вона ж є найбільш частою причиною смерті пацієнтів з цими захворюваннями.
Хоча медулярна карцинома частіше спостерігається у другому десятиріччі життя, в той же час, у дітей з МЕН-2В синдромом МКЩЗ може бути виявлена у віці 2-3 місяців. Існує низка особливостей перебігу медулярної карциноми щитовидної залози залежно від форми захворювання (спорадична або сімейна). На відміну від спорадичної медулярної карциноми, коли спостерігається однофокусне (одностороннє) ураження щитовидної залози, у хворих з сімейною формою МКЩЗ практично завжди є двостороннє ураження щитовидної залози з множинними пухлинними фокусами, які розташовані, як правило, у верхній частині органу.
МКЩЗ, пов’язана з МЕН-2В синдромом, відрізняється злоякіснішим перебігом, ніж спорадична або ж пов’язана з іншими синдромами. Доведено велику біологічну агресивність МКЩЗ при МЕН-2В синдромі.
На жаль, далеко не завжди діагноз МКЩЗ можна поставити на доклінічній стадії, особливо якщо не проводиться скринінг близьких родичів пацієнтів зі спадковими формами МКЩЗ. Більшість пацієнтів із МКЩЗ спочатку звертаються з приводу вузлів у щитоподібній залозі. Шийна лімфаденопатія може бути першою ознакою захворювання. Характерна особливість пухлини – тенденція до поширення в паратрахеальні та медіастинальні лімфовузли. Часто спостерігаються симптоми здушення в області органів дихання, викликані місцевим поширенням пухлини.
У 30% пацієнтів спостерігається водяниста діарея, яка буває вираженішою у пацієнтів із запущеними формами медулярної карциноми і, як правило, свідчить про поганий прогноз. Механізм діареї не відомий, але, ймовірно, вона викликається вивільненням пухлиною простагландину, серотоніну або кальцитоніну. 10% пацієнтів мають симптоми, пов’язані з віддаленими метастазами, особливо в кістки і легені. У пацієнтів з МЕН-2В синдромом появі змін з боку щитовидної залози зазвичай передує поява невром, які можуть спостерігатися на слизовій оболонці всіх ділянок шлунково-кишкового тракту. Тому першими можуть з’явитися скарги на запори або проноси. У таких хворих невроми можуть бути виявлені при біопсії ректальної області. Обстеження рогівки може виявити характерні потовщення корнеальних нервів, які стають помітними з перших днів життя. У постановці діагнозу МЕН-2В клінічно допомагає ряд аномалій, які спостерігаються у таких дітей. Хворі з цим синдромом мають дуже характерну зовнішність – «марфаноподібну» – видовжене обличчя, відстовбурчені вуха, товсті бугристі губи, які пояснюють невромами. Характерним для цих хворих є наявність широких, рідких зубів, третьої повіки, «готичного піднебіння». З числа аномалій скелету нерідко спостерігаються впала грудна клітина, кіфоз, вальгусна деформація колінних суглобів.
У 20-25% випадків синдрому МЕН-2А спостерігається паратиреоїдна гіперплазія. Найхарактернішою ознакою гіперпаратиреозу в рамках МЕН-2А є наявність безсимптомних або клінічно значимих каменів у сечовивідному тракті. Тяжкість гіперпаратиреозу при МЕН-2 значно поступається проявам цього захворювання при спорадичних формах і навіть при синдромі МЕН-1.
У 40-60% випадків синдрому МЕН-2А і 50% випадків синдрому МЕН-2В зустрічається феохромоцитома. Її особливістю є мультицентричність і двостороннє розташування. На відміну від спорадичної форми, феохромоцитома при синдромах МЕН, в основному, секретує адреналін.
Діагностика
Синдром МЕН 1 типу
Першою складовою в діагностиці зазвичай є гіперпаратиреоз (див. розділ 4). При підозрі на синдром МЕН-1 ведеться пошук інших компонентів синдрому, а саме:
- Визначення рівня іонізованого кальцію і паратгормону в сироватці крові.
- Визначення рівня пролактину.
- Визначення рівня гастрину, якщо він нормальний, натще; його вимірюють після прийому їжі або стимуляції секретином.
- Визначення рівня панкреатичного поліпептиду, інсуліну, глюкагону натще і після їжі. КТ або МРТ гіпофізу, черевної порожнини, наднирників.
Синдроми МЕН 2 типу
Діагностика МЕН-синдромів базується на генетичному скринінзі, біохімічних та клінічних ознаках цього захворювання.
Генетичний скринінг.
З 1993 року, коли була виявлена мутація в протоонкогені Ret в родинах з МЕН-2А, МЕН-2В і СМКЩЗ, з’явилася можливість ідентифікувати пацієнтів, що мають ризик розвитку МКЩЗ. За допомогою цього дослідження членів родин пацієнтів з МКЩЗ можна розділити на дві групи: ті, що мають ризик занедужати МКЩЗ і ті, у кого такого ризику немає. Це дозволяє з більшою впевненістю підходити до ведення пацієнтів групи ризику.
Більшість мутацій, пов’язаних з МЕН-2А і СМКЩЗ, зосереджені в багатому цистеїном регіоні рецептора Ret. Пацієнти з МЕН-2В мають одиничну крапкову мутацію в кодоні 918 Ret.
Пряме тестування ДНК – це високоточна методика виявлення родичів, що успадкували специфічну мутацію, пов’язану з МЕН-2А та МЕН-2В. У випадках, коли були виявлені зміни в геномі, характерні для МЕН-2 синдромів, ситуація доволі однозначна: гіперплазія С-клітин або ж медулярна карцинома щитовидної залози виявлена у всіх носіїв гена, навіть у наймолодших.
Особливо важливим є своєчасне (доклінічне) виявлення пацієнтів з МЕН-2В синдромом, тому що серед тих, кому діагноз було встановлено вже за наявності клінічних ознак і симптомів МКЩЗ, практично половина вмирає від цього захворювання, а інші страждають від тяжких проявів хвороби.
Тестування родичів першого ступеня пацієнтів з МКЩЗ слід починати у віці 3-5 років. У сім’ях з МЕН-2В скринінг має відбутися протягом першого року життя і повинен включати пошук характерного фенотипу.
Біохімічний скринінг
Для багатьох пухлин ендокринної системи, як доброякісних, так і злоякісних, характерна гіперпродукція гормонів, що є клінічним або біохімічним маркером розвитку хвороби і дозволяє на ранніх стадіях встановити діагноз. У випадку з медулярною карциномою злоякісні С-клітини виробляють надлишкову кількість кальцитоніну, поліпептиду, що складається з 32 амінокислот. Фізіологічна функція кальцитоніну в організмі людини вивчена недостатньо, але з’ясовано, що він пригнічує резорбцію кісткової тканини і може знижувати рівень кальцію сироватки. Проте пацієнти з МКЩЗ зазвичай мають нормальний рівень кальцію в сироватці.
Здатність клітин медулярної карциноми щитовидної залози виробляти кальцитонін широко використовується для обстеження пацієнтів з цим захворюванням. Хоча вимір базального рівня кальцитоніну проводиться досить обмежено, у практиці широко використовуються провокаційні тести, частіше за все – тест із пентагастрином або препаратами кальцію. Зараз найефективнішою вважається стимуляція викиду кальцитоніну одночасною інфузією пентагастрину та іонів кальцію (0,5 мкг/кг і 2 мг/кг відповідно). Пацієнтам із групи ризику по розвитку МЕН-2 слід проводити провокаційні тести на викид кальцитоніну, починаючи з трирічного віку.
Хоча з відкриттям мутації в гені С-ret роль біохімічного скринінгу МКЩЗ дещо зменшилася, вимір рівня кальцитоніну продовжують проводити в таких випадках:
- Для передопераційної діагностики МКЩЗ у пацієнтів з вузловим зобом.
- Для скринінгу близьких родичів хворих з МЕН-2А, МЕН-2В та СМКЩЗ на наявність МКЩЗ в тих випадках, коли тестування ДНК провести неможливо.
- Через те, що за клінічними ознаками й гістопатологічними дослідженнями не можна адекватно виключити спадкову МКЩЗ, пропонують проводити біохімічний скринінг у близьких родичів усіх пацієнтів із щойно виявленою МКЩЗ до тих пір, поки не будуть доступні генетичні маркери для диференціювання сімейних і спорадичних форм.
- Визначення кальцитоніну є складовою частиною схеми ведення носіїв гену МЕН-2. У таких хворих відхилення від норми базального або стимульованого рівня кальцитоніну є явним показанням для тиреоїдектомії.
- По зниженню рівня кальцитоніну в післяопераційному періоді роблять висновок про радикальність проведеного лікування; його підвищення говорить про наявність рецидиву або метастазування.
Можливість використання результатів аналізу ДНК дозволила порівняти результати генетичного і біохімічного скринінгу. Були ідентифіковані носії гену, що мають нормальні значення стимуляційного тесту С-клітин, у яких були знайдені МКЩЗ невеликих розмірів. Таким чином, в доклінічній стадії захворювання не можна достовірно встановити діагноз МКЩЗ користуючись лише біохімічними методами діагностики. Ці результати свідчать про необхідність рутинного проведення аналізу Ret-протоонкогену при ухваленні рішення про проведення тиреоїдектомії.
Встановлення діагнозу МКЩЗ за допомогою загальноприйнятих методів обстеження (УЗД щитовидної залози, тонкоголкова аспіраційна біопсія, а також визначення рівня кальцитоніну в сироватці крові) можливе лише за наявності клінічних проявів. У хворих зі спадковими формами медулярної карциноми щитовидної залози, приймаючи до уваги її агресивніший перебіг, цей діагноз може і повинен ставитися на доклінічній стадії (за наявності настороженості до даного захворювання, обізнаності з особливостями його перебігу, ретельному спостереженні за членами родин пацієнтів з медулярною карциномою щитовидної залози). Проведення ж молекулярно-генетичного дослідження дозволяє виділити членів сімей, що мають спадкову схильність до МКЩЗ. Найдоцільнішим є проведення дослідження членів родин таких пацієнтів на наявність мутації в Rеt-протоонкогені.
Усім пацієнтам з МЕН показане обстеження на наявність феохромоцитоми, яке слід розпочинати у віці 5 років і продовжувати протягом усього життя. Діагноз феохромоцитоми у хворих з наявністю таких яскравих проявів, як симпато-адреналові кризи, не складний. Через можливі ускладнення при операціях з приводу МРЩЗ, пов’язаних з гемодинамічними кризами, важливим моментом є виявлення асимптоматичних феохромоцитом. У цих хворих ранній діагноз залежить від ретельного збору скарг, анамнезу, визначення рівня катехоламінів у крові й сечі, проведення топічної діагностики.
Лікування
Вибір лікування при МЕН визначається клінічними проявами захворювання, особливостями росту пухлин і можливими ускладненнями. План лікування складають з урахуванням всіх компонентів синдрому. Чим раніше поставлений діагноз і чим радикальніші методи лікування застосовувалися, тим кращий прогноз і вищі шанси вилікувати хворого.
МЕН-1
Вибір лікування визначається клінічними проявами захворювання, особливостями росту пухлин. Враховуючи, що пухлини в рамках цього синдрому, як правило, багатовогнищеві, то при виявленні пухлин, залежно від локалізації, проводять резекцію пухлини. Одночасно проводять паратиреоїдектомію з аутотрансплантацією однієї із залоз. Якщо гіпергастринемія була зумовлена не гастриномою, а гіперпаратиреозом, вона зникає або істотно зменшується після паратиреоїдектомії.
МЕН-2
Перед проведенням хірургічного лікування медулярного раку щитовидної залози слід виключити у пацієнта наявність феохромоцитоми. Якщо доведена патологія мозкової речовини наднирників, адреналектомію слід провести перед тиреоїдектомією для попередження гіпертонічної кризи під час операції. Зважаючи на те, що єдиний ефективний спосіб лікування МКЩЗ – оперативний, успішний результат залежить від раннього діагнозу і лікування, до того, як пухлина метастазує в регіонарні лімфовузли або ж дистально. Первинною операцією при МКЩЗ повинна бути тотальна тиреоїдектомія з видаленням лімфовузлів шиї. Після тиреоїдектомії хворим призначається супресивна терапія тиреоїдними гормонами. Лікування рецидивів або метастатичних уражень насамперед оперативне, включаючи паліативні операції, мікродисекцію. Радіаційна терапія використовується для лікування метастазів у кістки або ж метастазів, що не можуть бути видалені оперативним шляхом. Ефективність доступних програм хіміотерапії не встановлена.
Профілактична тиреоїдектомія
Рання діагностика пацієнтів із сімейними формами медулярної карциноми щитовидної залози шляхом генетичного скринінгу членів сімей дозволяє проводити лікування за допомогою тиреоїдектомії до появи клінічних і біохімічних проявів МКЩЗ.
До широкого розвитку генетичних методів діагностики вважалося, що слід постійно контролювати рівень кальцитоніну у дітей з родин із МЕН-2 синдромом для раннього виявлення пухлини. Однак було показано, що базальний і стимульований рівень кальцитоніну не може використовуватися як критерій вибору часу оперативного втручання у дітей з синдромом МЕН-2. Хірургічне лікування слід проводити в ранньому дитинстві на підставах результатів молекулярно-генетичного тестування. Частота виявлення МРЩЗ при превентивній тиреоїдектомії доволі чітко корелює з віком: чим в молодшому віці проведене видалення щитовидної залози, тим менше виражені ознаки МРЩЗ в гістологічному препараті. На сучасному етапі розвитку хірургії післяопераційні ускладнення зустрічаються рідко.
Умови, в яких слід надавати медичну допомогу
Постановка діагнозу і лікування має проводитися в спеціалізованих ендокринологічних стаціонарах; після локалізації пухлин лікування має проводитися у відділенні ендокринної хірургії, відділенні хірургії гастроентерального профілю, нейрохірургічного або онкологічного профілю. Ендокринолог, педіатр в поліклінічному відділенні проводить подальше спостереження за станом хворого і організовує заходи, спрямовані на виявлення нових вірогідних компонентів синдрому.
Перелік і обсяг медичних послуг обов’язкового асортименту
Огляд дитячого ендокринолога, молекулярно-генетичне дослідження RET-протоонкогену при МЕН-2 синдромі, спадковій і/або двосторонній феохромоцитомі, медулярному раці щитовидної залози. За наявності підозри або при підтвердженому діагнозі МЕН-синдрому – проведення комплексу клініко-лабораторних досліджень, спрямованих на виявлення вірогідних компонентів даного синдрому: визначення базального і стимульованого рівня кальцитоніну (при МЕН-2 синдромах), рівнів загального та іонізованого кальцію, фосфору, ПТГ сироватки, екскреції кальцію і фосфору з сечею, сечовини і креатиніну сироватки, загальні аналізи крові та сечі, УЗД та ТАПБ щитовидної залози, нирок, візуалізація пухлин (УЗД, КТ, МРТ), огляд хірурга і т.д.
Перелік і обсяг додаткових медичних послуг
Консультація нефролога, ортопеда, нейрохірурга, моніторинг АТ.
Можливі результати надання медичної допомоги
Прогноз при МЕН 1 типу залежить від своєчасної діагностики і радикальності оперативного лікування.
Прогноз при МЕН-2 синдромах пов’язаний зі ступенем поширеності МКЩЗ та з наявністю і ступенем тяжкості іншого компоненту синдромів – феохромоцитоми.
Загальна смертність при синдромі МЕН-2В значно вища, аніж при МЕН-2А. Середній вік хворих з МЕН-2А – 60 років, тоді як у хворих з МЕН 2В – 30 років. Висока смертність зумовлена злоякісним перебігом і швидким розвитком метастазів медулярного раку щитовидної залози.
Характеристика кінцевого очікуваного результату лікування
У результаті лікування досягається зменшення або, при можливості, зникнення клінічних проявів пухлин, відсутність метастазування медулярної карциноми щитовидної залози й інших пухлин за рахунок раннього і своєчасного оперативного втручання, поліпшення стану хворих.
Вимоги до дієтичних призначень та обмежень
Вимоги до дієтичних призначень диктуються в кожному окремому випадку пацієнта з МЕН-синдромом, наявністю і вираженістю окремих його компонентів.
- Категорії статей
- Інвалідність
- Інфекційні захворювання
- Акушерство, гінекологія, репродуктивна медицина
- Алергія
- Варікоз
- Гастроентерологія
- Гепатологія
- Головний біль
- Депресія. Психотерапія
- Дерматокосметологія
- Дитяча і підліткова гінекологія
- Дитяче харчування
- Ендокринологія. Цукровий діабет
- Кардіологія
- Мамологія
- Надлишкова вага. Дієти
- Неврологія
- Онкологія
- Отоларингологія
- Офтальмологія
- Проктологія
- Пульмонологія, фтизіатрія
- Стоматологія. Захворювання порожнини рота
- Травматологія і ортопедія
- Урологія і нефрологія
- Школа здоров'я
- Щеплення

 Рак яичников: причины, симптомы, методы лечения
Рак яичников: причины, симптомы, методы лечения
 Критерии качества жизни в медицине и кардиологии
Критерии качества жизни в медицине и кардиологии
 Рак щитоподібної залози: уроки останніх десятиріч
Рак щитоподібної залози: уроки останніх десятиріч
 Таргетная терапия: продление и улучшение качества жизни у больных раком молочной железы
Таргетная терапия: продление и улучшение качества жизни у больных раком молочной железы