Селлсепт инструкция, аналоги и состав
Склад:
діюча речовина: mycophenolic acid;
1 капсула містить мофетилу мікофенолату 250 мг;
допоміжні речовини: крохмаль кукурудзяний прежелатинізований, кроскармелоза натрію, повідон (К90), магнію стеарат; капсула: желатин, натрію лаурилсульфат, натрію карбоксиметилцелюлоза, кремнію діоксид, титану діоксид, індигокармін, заліза оксид червоний, заліза оксид жовтий.
Лікарська форма. Капсули.
Фармакотерапевтична група. Селективні імуносупресивні препарати. Кислота мікофенолова.
Код АТС L04AA06.
Клінічні характеристики.
Показання.
Профілактика гострого відторгнення органа та лікування рефрактерного до терапії відторгнення органа у хворих після алогенної трансплантації нирки.
Профілактика гострого відторгнення органа та поліпшення виживаності трансплантату і виживаності пацієнтів після алогенної трансплантації серця.
Профілактика гострого відторгнення органа у хворих після алогенної трансплантації печінки.
Протипоказання.
Гіперчутливість до мофетилу мікофенолату, мікофенольної кислоти та інших компонентів препарату. Вагітність.
Спосіб застосування та дози.
Профілактика відторгнення нирки.
Перша доза Селлсепту повинна бути застосована протягом 72 год після трансплантації. Хворим із нирковими трансплантатами рекомендується прийом по 1 г двічі на добу (добова доза 2 г). У клінічних дослідженнях застосовувалася доза в 1,5 г двічі на добу (добова доза 3 г), що не давала переваги у плані ефективності, хоча також була безпечною. У хворих, котрі застосовували 2 г Селлсепту на добу, профіль безпеки був у цілому краще, ніж у тих, які застосовували добову дозу 3 г. Селлсепт повинен призначатися одночасно зі стандартною терапією циклоспорином і кортикостероїдами.
Лікування рефрактерного відторгнення нирки.
Як для початкового лікування рефрактерного до терапії іншими імуносупресорами гострого клітинно-опосердкованого відторгнення, так і для підтримуючої терапії хворим рекомендується добова доза в 3 г (1,5 г 2 рази на добу). Селлсепт повинен призначатися одночасно зі стандартною терапією циклоспорином і кортикостероїдами.
Профілактика відторгнення серця.
Перша доза Селлсепту повинна бути застосована протягом 5 днів після трансплантації. Рекомендований режим дозування – по 1,5 г 2 рази на добу.
Профілактика відторгнення печінки.
Перша доза Селлсепту повинна бути застосована якомога швидше після трансплантації. Рекомендований режим дозування – по 1,5 г 2 рази на добу.
Побічні реакції.
Дані клінічних досліджень
Профіль побічних дій, пов'язаних із застосуванням імуносупресорів, часто важко встановити через наявність основного захворювання та одночасного застосування багатьох інших лікарських засобів. Основними побічними реакціями, пов'язаними із застосуванням Селлсепту в комбінації з циклоспорином і кортикостероїдами, є діарея, лейкопенія, сепсис і блювання; існують також дані про підвищення частоти деяких видів інфекцій. Профіль безпеки Селлсепту при лікуванні рефрактерної трансплантації нирки був аналогічний у трьох контрольованих дослідженнях із профілактики відторгнення нирки при використанні препарату в дозі 3 г на добу. Діарея і лейкопенія з наступною анемією, нудота, блювання, диспепсія, біль у животі та сепсис - найпоширеніші побічні реакції, що зустрічалися у хворих, які приймали Селлсепт частіше, ніж у хворих, котрі застосовували внутрішньовенно кортикостероїди.
У контрольованих дослідженнях з профілактики відторгнення нирки протягом 3 років після пересадки лімфопроліферативні захворювання або лімфоми розвилися у 1,6 % хворих, які застосовували Селлсепт у дозі 3 г на добу, і в 0,6 % – у дозі 2 г на добу, у той час як у групі плацебо цей показник становив 0 %, а в групі азатіоприну – 0,6 %. У контрольованих дослідженнях з лікування рефрактерного відторгнення нирки частота лімфом при середньому періоді спостереження до 42 місяців становила 3,9 %.
Після трансплантації серця частота лімфопроліферативних захворювань при прийомі Селлсепту в дозі 3 г на добу дорівнювала 0,7 %, при лікуванні азатіоприном – 2,1 %. Після трансплантації серця частота раку шкіри (крім меланоми) при прийомі Селлсепту в дозі 3 г на добу становила 5,5 %, при лікуванні азатіоприном – 6,9 %. Після трансплантації серця за пацієнтами ретельно спостерігали протягом 3 років, причому за 26 % пацієнтами спостерігали менше року, а 34 % – більше 2 років.
Після трансплантації печінки в ході спостереження тривалістю не менш 1 року частота лімфопроліферативних захворювань або лімфом при прийомі Селлсепту в дозі 3 г на добу дорівнювала 0,4 %, при прийомі азатіоприну – 0 %. Карциноми шкіри розвилися у 2,2 % пацієнтів, які приймали Селлсепт, і в 2,1 %, які застосовували азатіоприн.
Ризик опортуністичних інфекцій був підвищений у всіх пацієнтів і зростав зі збільшенням сумарної дози імунодепресантів. Загальна частота опортуністичних інфекцій після трансплантації нирки і печінки у хворих, які застосовували Селлсепт і азатіоприн, була однаковою. Після трансплантації серця загальна частота опортуністичних інфекцій при лікуванні Селлсептом була приблизно на 10 % вище, ніж при прийомі азатіоприну, однак смертність від інфекцій або сепсису у хворих, які застосовували Селлсепт, не збільшувалася. При прийомі Селлсепту після трансплантації серця частіше відзначалися кандидоз шкіри і слизових оболонок, герпесвірусні інфекції, спричинені H.simplex, H.zoster, цитомегаловірусом. У пацієнтів після трансплантації печінки кількість випадків інфекції, обумовленої H.simplex, також була більша, ніж у групі лікованих азатіоприном.
У хворих літнього віку при лікуванні Селлсептом у рамках комбінованої терапії ризик деяких інфекцій (включаючи тканинні інвазивні форми маніфестної цитомегаловірусної інфекції), а також, шлунково-кишкових кровотеч і набряку легень вище, ніж у пацієнтів більш молодшого віку.
При застосуванні препарату спостерігалися такі небажані явища, як коліт (іноді цитомегаловірусної етіології), панкреатит, підвищення частоти тяжких інфекцій (менінгіту, інфекційного ендокардиту, туберкульозу та атипічних мікобактеріальних інфекцій).
Організм у цілому (≥10 %): астенія, гарячка, головний біль, інфекції, болі (у животі, попереку, грудній клітці), периферичні набряки, сепсис, асцит, здуття живота, грижі, перитоніт, гикавка. 3 - 10 %: кісти (у тому числі лімфоцеле й гідроцеле), набряки обличчя, грипоподібний синдром, кровотечі, грижі, болі в області таза, целюліт, біль у шиї, блідість шкірних покривів.
Система крові й лімфатична система (≥ 10 %): анемія (у тому числі гіпохромна), лейкоцитоз, лейкопенія, тромбоцитопенія, екхімози. 3 - 10 %: екхімози, збільшення протромбінового й тромбопластинового часу, панцитопенія.
Сечостатева система ≥ 10 %: гематурія, некроз ниркових канальців, інфекції сечовивідних шляхів, порушення функції нирок, олігурія.
3 - 10 %: альбумінурія, дизурія, гідронефроз, імпотенція, пієлонефрит, часте сечовипускання, гематурія, ніктурія, ниркова недостатність, нетримання й затримка сечі; гостра ниркова недостатність, набряк мошонки.
Серцево-судинна система ≥ 10 %: артеріальна гіпертензія, аритмія, брадикардія, серцева недостатність, артеріальна гіпотекція, перикардіальний випіт.
3 - 10 %: стенокардія, артеріальна гіпотензія, у тому числі ортостатична, тахікардія, брадикардія, тромбоз, втрата свідомості, вазодилатація; аритмії (суправентрикулярні й шлуночкові екстрасистоли, мерехтіння й тріпотіння передсердь, суправентрикулярні й шлуночкові тахікардії), зупинка серця, застійна серцева недостатність, легенева гіпертензія, вазоспазм, підвищення венозного тиску.
Обмін речовин (≥ 10 %): ацидоз (метаболічний або респіраторний), збільшення маси тіла, гіперволемія; порушення загоєння ран.
3 - 10 %: після трансплантації нирки: ацидоз (метаболічний або респіраторний), збільшення маси тіла, дегідратація, гіперволемія, подагра, гіповолемія, гіпоксія, спрага, схуднення, алкалоз.
Лабораторні показники (≥10 %): гіперглікемія, гіперкаліємія, гіпокаліємія, гіпофосфатемія; гіпербілірубінемія, підвищення залишкового азоту, підвищення креатиніну, підвищення активності ферментів ЛДГ, АСТ, АЛТ у сироватці крові, гіперхолестеринемія, гіперліпідемія, гіперурикемія, гіпомагніємія, гіпонатріємія, гіпокальціємія, гіпопротеїнемія.
3 - 10 %: підвищення активності лужної фосфатази, гамма-глютамілтранспептидази, ЛДГ, АСТ і АЛТ у сироватці крові, підвищення креатиніну сироватки крові, гіперкальціємія, гіперліпідемія, гіпокальціємія, гіпоглікемія, гіпопротеїнемія, гіперурикемія, гіпохлоремія, гіпофосфатемія; гіпонатріємія.
Шлунково-кишковий тракт > 10 %: диспепсія, блювання, запор, діарея, кандидоз ротової порожнини, холангіт, холестатичнина жовтуха, гепатит, анорексія. 3 - 10 %: дисфагія, гінгівіт, гіперплазія ясен, стоматит, езофагит, гастрит, гастроентерит, шлунково-кишкові кровотечі, виразка шлунка, кишкова непрохідність, мелена, ураження прямої кишки, кандидоз шлунково-кишкового тракту.
Органи дихання ≥ 10 %: посилення кашлю, задишка, фарингіт, пневмонія, бронхіт; бронхіальна астма, плевральний випіт, риніт, синусит; ателектаз.
3 - 10 %: астма, плевральний випіт, набряк легень, риніт, синусит, апное, ателектаз, бронхіт, носові кровотечі, кровохаркання, новоутворення, пневмоторакс, набряк легень, посилення виділення мокротиння, зміна голосу, гіпервентиляція, кандидоз дихальних шляхів, риніт.
Шкіра і її придатки ≥ 10 %: акне, простий герпес, оперізуючий лишай, висип, свербіж, підвищена пітливість.
3 - 10 %: випадіння волосся, доброякісні новоутворення шкіри, грибковий дерматит, простий герпес, оперізувальний лишай, гірсутизм, свербіж, рак шкіри, гіпертрофія шкіри, підвищена пітливість, шкірні виразки, висип, підвищена пітливість, акне, крововиливи, везикулобульозні висипи.
Нервова система ≥ 10 %: запаморочення, безсоння, тремор; психомоторне збудження, тривога, сплутаність свідомості, депресія, гіпертонус, парестезії, сонливість, тремор.
3 - 10 %: психомоторне збудження, депресія, гіпертонус скелетної мускулатури, парестезії, сонливість; судоми, емоційна лабільність, галюцинації, нейропатія, запаморочення; делірій, сухість у роті, нейропатія, психоз, порушення мислення.
Кістково-м'язова система ≥ 10 %: судоми в ногах, біль у м'язах, м'язова слабкість.
3 - 10 %: болі в суглобах, судоми в ногах, болі в м'язах, м'язова слабкість, остеопороз.
Органи відчуття ≥ 10 %: амбліопія.
3 - 10 %: амбліопія, катаракта, кон’юнктивіт, порушення зору, глухота, біль у вухах, крововилив в око, вестибулярні запаморочення.
Ендокринна система 3 - 10 %: цукровий діабет, захворювання паращитовидних залоз, синдром Кушинга, гіпотиреоз.
При профілактиці відторгнення ниркового трансплантату профіль безпеки ММФ в добовій дозі 2 г був дещо кращим, ніж у добовій дозі 3 г.
Післяреєстраційне застосування препарату
Органи травлення: коліт (іноді цитомегаловірусної етіології), панкреатит, окремі випадки атрофії кишкових ворсин.
Імунна система: окремі випадки тяжких, що загрожують життю інфекцій (менінгіту, інфекційного ендокардиту), підвищення частоти деяких інфекцій типу туберкульозу й атипових форм мікобактеріальних інфекцій.
Передозування.
Даних про передозування мофетилу мікофенолату у людини немає.
2-морфоліновий ефір мікофенолової кислоти не можна видалити з організму методом гемодіалізу, однак при високих концентраціях глюкороніду 2-морфолінового ефіру мікофенолової кислоти у плазмі (> 100 мкг/моль), невеликі його кількості все-таки виводяться. Препарати, що зв'язують жовчні кислоти, наприклад, холестирамін, можуть сприяти виведенню 2-морфолінового ефіру мікофенолової кислоти з організму, збільшуючи його екскрецію.
Застосування у період вагітності або годування груддю.
Препарат не рекомендується застосовувати вагітним через тератогенний вплив на плід людини. Селлсепт може бути призначений лікарем лише у виняткових випадках, коли потенційна користь для матері перевищує можливий ризик для плода. Терапію Селлсептом не слід починати доти, доки не отриманий негативний результат обстеження на вагітність. До початку терапії Селлсептом, у ході лікування і протягом 6 тижнів після його закінчення обов'язковим є використання ефективних методів контрацепції, навіть якщо в анамнезі жінки зазначена безплідність (за винятком перенесеної гістеректомії). Якщо утримання від статевого життя не можливе, необхідно використовувати два надійних методи контрацепції одночасно. У разі вагітності в ході терапії необхідно обговорити бажаність її збереження з лікарем.
Не відомо, чи виділяється Селлсепт із жіночим молоком. Оскільки з жіночим молоком екскретуються багато препаратів, а також у зв'язку з можливістю серйозних побічних реакцій на мофетилу мікофенолат у немовлят, питання про продовження годування груддю або прийомом препарату вирішує лікар з урахуванням важливості лікування для матері.
Діти. Безпечність та ефективність препарату для хворих дитячого віку не встановлена. Фармакокінетичні дані щодо дітей, які перенесли трансплантацію нирки, досить обмежені, а щодо дітей після трансплантації серця або печінки відсутні.
Особливі заходи безпеки.
Оскільки мофетилу мікофенолат в експерименті на щурах і кролях виявив тератогенну дію, капсули Селлсепту не слід відкривати або розламувати. Необхідно уникати вдихання порошку, що міститься в капсулах Селлсепту, або його прямого потрапляння на шкіру або слизові оболонки. Якщо це відбулося, потрібно ретельно промити уражену ділянку водою з милом, а очі - лише водою.
Особливості застосування.
При нейтропенії (абсолютне число нейтрофілів < 1300 в 1 мкл) необхідно перервати лікування Селлсептом або зменшити його дозу і ретельно спостерігати за станом пацієнта.
У хворих із тяжкою хронічною нирковою недостатністю (швидкість клубочкової фільтрації менш ніж 25 моль/хв/1,73 м2) поза найближчим посттрансплантаційним періодом або після терапії з приводу гострого або рефрактерного відторгнення варто уникати доз вище 2 г на добу. За цими хворими потрібно ретельно спостерігати.
Дані про ефективність препарату для пацієнтів з тяжкою нирковою недостатністю, які перенесли пересадку серця або печінки, відсутні.
Корекція дози хворим із затримкою функції ниркового трансплантата не потрібна.
Хворим, котрі перенесли трансплантації нирки і печінки з тяжкими ураженнями, корекція дози не потрібна. Дані про ефективність препарату для пацієнтів з тяжкими ураженнями печінки, які перенесли трансплантації серця, відсутні.
Для хворих літнього віку (≥ 65 років), які перенесли пересадку нирки, серця або печінки, рекомендується доза 1 г 2 рази на добу.
Як і на тлі комбінованої імуносупресії взагалі, при призначенні мофетилу мікофенолату як компонента імуносупресивної схеми є підвищений ризик розвитку лімфом і інших злоякісних новоутворень, особливо шкіри (див. "Побічні реакції"). Цей ризик пов'язаний не із застосуванням будь-якого препарату як такого, а з інтенсивністю й тривалістю імуносупресії.
Хворим із підвищеним ризиком раку шкіри з метою обмежити вплив сонячних і ультрафіолетових променів слід носити відповідний закритий одяг й використовувати сонцезахисні креми з високим значенням захисного фактора.
Хворі, які застосовують мофетилу мікофенолат, повинні бути проінформовані про необхідність відразу ж повідомляти лікаря про будь-які ознаки інфекції, кровоточивості, кровотеч або інших ознаках пригнічення кісткового мозку. Надмірне пригнічення імунної системи може також підвищити чутливість до інфекцій, в тому числі до опортуністичних, сепсису та інших інфекцій із летальним наслідком. Під час лікування мофетилом мікофенолатом вакцинація може бути менш ефективною, необхідно уникати живих ослаблених вакцин. Можна проводити вакцинацію проти грипу у відповідності до національних рекомендацій.
Так як застосування мофетилу мікофенолату може супроводжуватись побічними реакціями з боку шлунково-кишкового тракту, необхідно з обережністю призначати препарат пацієнтам з захворюваннями шлунково-кишкового тракту у стадії загострення.
Мофетилу мікофенолат є інгібітором інозинмонофосфатдегідрогенази, тому не слід призначити його пацієнтам із рідкісним генетично обумовленим спадковим дефіцитом гіпоксантингуанінфосфорибозилтрансферази (синдроми Леша-Найєна і Келлі-Зигміллера). Мофетилу мікофенолат не рекомендується призначати одночасно з азатіоприном, так як обидва препарати пригнічують кістковий мозок та їх одночасне застосування не вивчалось.
Необхідно дотримуватись обережності при одночасному прийомі мофетилу мікофенолату з препаратами, що впливають на печінково-кишкову циркуляцію, так як вони можуть знизити ефективність мофетилу мікофенолату.
Лабораторний контроль: при лікуванні мофетилом мікофенолатом необхідно визначати розгорнуту формулу крові протягом першого місяця – щотижнево, протягом другого і третього місяців лікування – 2 рази на місяць, а потім протягом першого року – щомісячно.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Препарат не впливає на швидкість реакції при керуванні транспортними засобами та роботі з машинами і складними механізмами.
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Ацикловір. При призначенні мофетилу мікофенолату разом з ацикловіром спостерігалися більш високі концентрації глюкороніду 2-морфолінового ефіру мікофенолової кислоти та ацикловіру в плазмі, ніж при призначенні кожного препарату окремо. Оскільки плазмові концентрації глюкороніду 2-морфолінового ефіру мікофенолової кислоти, як і ацикловіру, підвищуються при нирковій недостатності, є ймовірність, що ці два препарати конкурують відносно канальцевої секреції, що може спричинити подальше підвищення концентрації обох лікарських препаратів.
Антациди, що містять гідроокис магнію та алюмінію: при прийомі разом з антацидами всмоктування мофетилу мікофенолату зменшується.
Холестирамін: після призначення разової дози в 1,5 г мофетилу мікофенолату здоровим добровольцям, які попередньо застосовували по 4 г холестираміну 3 рази на добу протягом 4 днів, спостерігалося зменшення AUCМФК на 40 %. Необхідно бути обережним при одночасному призначенні мофетилу мікофенолату і препаратів, що впливають на печінково-кишкову рециркуляцію.
Циклоспорин А: мофетилу мікофенолат не впливає на фармакокінетику циклоспорину А.
Азатіоприн: одночасне призначення із Селлсептом не рекомендується, тому що їхній сумісний прийом не вивчався.
Ганцикловір: за результатами дослідження з разовим пероральним прийомом рекомендованих доз мофетилу мікофенолату і внутрішньовенним введенням ганцикловіру, з урахуванням відомого впливу ниркової недостатності на фармакокінетику мофетилу мікофенолату і ганцикловіру, можна припустити, що одночасне застосування цих препаратів (що конкурують у процесі канальцевої секреції) спричинить підвищення концентрацій глюкороніду 2-морфолінового ефіру мікофенолової кислоти і ганцикловіру. Істотної зміни фармакокінетики 2-морфоліноетилового ефіру мікофенолової кислоти не очікується, тому коригувати дозу мофетилу мікофенолату не потрібно. Якщо мофетилу микофенолат і ганцикловір призначають хворим із нирковою недостатністю, необхідно дотримуватися рекомендованого для ганцикловіру режиму дозування і ретельно спостерігати за хворими.
Пероральні контрацептиви: Селлсепт не впливає на фармакокінетику пероральних контрацептивів. У ході досліджень з одночасним призначенням Селлсепту у дозі 1 г 2 рази на добу і комбінованих пероральних контрацептивів, що містять етинілестрадіол (0,02 - 0,04 мг) і левоноргестрел (0,05 - 0,2 мг), дезогестрел (0,15 мг) або гестродин (0,05 - 0,1 мг), 18 жінкам із псоріазом протягом 3 менструальних циклів не виявлено клінічно значимого впливу Селлсепту на сироваткові концентрації прогестерону, лютеїнізувального та фолікулостимулювального гормонів. Це свідчить про відсутність впливу Селлсепту на пригнічення овуляції під дією пероральних контрацептивів.
Триметоприм/сульфаметоксазол: не впливають на біодоступність 2-морфоліноетилового ефіру мікофенолової кислоти.
Такролімус: після того, як циклоспорин заміняли на такролімус у хворих зі стабільно функціонуючим нирковим трансплантатом, AUCМФК збільшувалася на 30 %, а AUCМФКГ зменшувалася приблизно на 20 %. Максимальна концентрація 2-морфоліноетилового ефіру мікофенолової кислоти не змінювалась, а глюкороніду 2-морфолінового ефіру мікофенолової кислоти – знижувалася на 20 %. Частково механізм цього ефекту може бути обумовлений посиленням біліарної секреції глюкороніду 2-морфолінового ефіру мікофенолової кислоти у поєднанні з посиленням ентерогепатичної циркуляції 2-морфолінового ефіру мікофенолової кислоти, оскільки підвищення концентрацій 2-морфоліноетилового ефіру мікофенолової кислоти після призначення такролімусу було більш вираженим ближче до кінця кривої «концентрація–час» (через 4 - 12 год після прийому). У хворих, які застосовують такролімус, доза Селлсепту не повинна перевищувати 1 г 2 рази на добу. За пацієнтами слід ретельно спостерігати. В іншому дослідженні у хворих після трансплантації нирки Селлсепт не впливав на концентрацію такролімусу.
Дані щодо фармакокінетики 2-морфоліноетилового ефіру мікофенолової кислоти у хворих після пересадки печінки при одночасній терапії Селлсептом і такролімусом дуже обмежені. У дослідженні ефекту Селлсепту на фармакокінетику такролімусу у хворих зі стабільним печінковим трансплантатом AUC такролімусу після багаторазового прийому Селлсепту в дозі 1,5 г 2 рази на добу зростала приблизно на 20 %.
Інші взаємодії: блокатори канальцієвої секреції (пробенецид) підвищують концентрацію глюкороніду 2-морфолінового ефіру мікофенолової кислоти.
Живі вакцини: не повинні вводитися пацієнтам у стані імунодепресії. Антитілоутворення у відповідь на інші вакцини може бути знижено.
Фармакологічні властивості.
Фармакодинаміка. Мофетилу мікофенолат – це 2-морфоліноетиловий ефір мікофенолової кислоти. 2-морфоліноетиловий ефіру мікофенолової кислоти – потужний селективний неконкурентний і оборотний інгібітор інозинмонофосфатдегідрогенази, що пригнічує синтез гуанозинових нуклеотидів de novo. Механізм, шляхом якого 2-морфоліноетиловий ефір мікофенолової кислоти пригнічує ферментну активність інозинмонофосфатдегідрогенази пов'язаний із тим, що 2-морфоліноетиловий ефір мікофенолової кислоти структурно імітує як кофактор нікотинаміддинуклеотидфосфат, так і каталізуючу молекулу води. Це перешкоджає окисненню інозинмонофосфату у ксантозо-5-монофосфат – дуже важливий етап біосинтезу гуанозинових нуклеотидів de novo. 2-морфоліноетиловий ефір мікофенолової кислоти має більш виражену цитостатичну дію на лімфоцити, ніж на інші клітини, оскільки проліферація Т- і В-лімфоцитів сильно залежить від синтезу пуринів de novo, у той час як клітини інших типів можуть переходити на обхідні шляхи метаболізму.
Фармакокінетика.
Всмоктування.
Після перорального прийому відбувається швидке і повне всмоктування і повний передсистемний метаболізм мофетилу мікофенолату з утворенням активного метаболіту мікофенолової кислоти. Біодоступність мофетилу мікофенолату при пероральному прийомі, відповідно до величини AUCМФК (площа під кривою "концентрація-час"), становить у середньому 94 % від такої ж при його внутрішньовенному введенні. Після перорального прийому концентрації мофетилу мікофенолату в плазмі не визначаються у зв'язку з його швидким перетворенням в активні метаболіти – 2-морфоліноетиловий ефір мікофенолової кислоти та інші.
У ранньому посттрансплантаційному періоді (до 40 днів після трансплантації нирок, серця або печінки) середні величини AUCМФК були приблизно на 30 %, а максимальні концентрації – приблизно на 40 % нижчими, ніж у пізньому посттрансплантаційному періоді (3 - 6 місяців після трансплантації).
Прийом їжі не впливає на ступінь всмоктування мофетілу мікофенолату (AUCМФК) при його призначенні по 1,5 г два рази на добу хворим після трансплантації нирки. Однак максимальна концентрація 2-морфоліноетилового ефіру мікофенолової кислоти при застосуванні препарату під час їжі знижується на 40 %.
Розподіл.
Як правило, приблизно через 6 - 12 год після прийому препарату спостерігається вторинне підвищення концентрації 2-морфоліноетилового ефіру мікофенолової кислоти у плазмі, що свідчить про ентерогепатичну циркуляцію препарату. У клінічно значимих концентраціях 2-морфоліноетилового ефіру мікофенолової кислоти на 97 % зв'язується з альбуміном плазми.
Метаболізм.
2-морфоліноетиловий ефір мікофенолової кислоти метаболізується в основному під дією глюкуронілтрансферази з утворенням фармакологічно неактивного фенольного глюкуроніду 2-морфоліноетилового ефіру мікофенолової кислоти. In vivo глюкоронід 2-морфолінового ефіру мікофенолової кислоти перетворюється у вільний 2-морфоліноетиловий ефір мікофенолової кислоти у ході ентерогепатичної циркуляції.
Виведення.
Незначні кількості препарату (< 1 % дози) виводяться із сечею у вигляді 2-морфоліноетилового ефіру мікофенолової кислоти. Після перорального прийому радіоактивно міченого мофетілу мікофенолату 93 % отриманої дози виділяється із сечею, а 6 % – з калом. Значна частина (близько 87 %) введеної дози виводиться із сечею у вигляді глюкороніду 2-морфолінового ефіру мікофенолової кислоти.
Фармацевтичні характеристики.
Основні фізико-хімічні властивості: тверді желатинові капсули, корпус – непрозорий, коричневого кольору, ковпачок – непрозорий, синього кольору; маркування чорного кольору: "CellCept 250" – на ковпачку та "Roche" – на корпусі; вміст капсул – гранульований порошок майже білого кольору.
Термін придатності. Термін придатності – 3 роки.
Умови зберігання. Зберігати у захищеному від світла, вологи та недоступному для дітей місці; температуру зберігання дивись на упаковці.

 Остеопороз в практике терапевта
Остеопороз в практике терапевта
 Бисфосфонаты: роль ибандроновой кислоты в лечении постменопаузального остеопороза
Бисфосфонаты: роль ибандроновой кислоты в лечении постменопаузального остеопороза
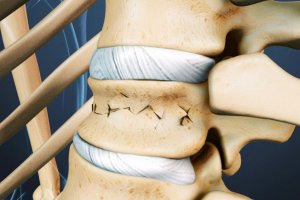 Остеопороз и заболевания пародонта (начало)
Остеопороз и заболевания пародонта (начало)
 Остеопороз: упал, очнулся – гипс
Остеопороз: упал, очнулся – гипс